|
|
|
���л�ѧ֪ʶ����ɡ����ʵ��������⼼�ɣ�2019�����°棩(��)
2019-05-30 04:12:48
�� �� �� ��
|
1��ѡ���� ��NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ� ��
A������NA����ԭ�ӵĺ����ڱ�״���µ����ԼΪ11.2L
B��25�棬1.01��105Pa��64gSO2�����к��е�ԭ����Ϊ3NA
C���ڳ��³�ѹ�£�11.2L Cl2���еķ�����Ϊ0.5NA
D����״���£�11.2LH2O���еķ�����Ϊ0.5NA
|
2��ѡ���� ��ʾ�����ӵ�������������������ȷ����
A����״���£�2.24L���ȼ��麬�з�����ĿΪ0.1NA
B��1 mol FeI2������������Ӧ��ת�Ƶĵ�����Ϊ2 NA
C��1 molCH3COONa ������CH3COOH����ˮ����������Һ�У�CH3COO����ĿΪNA
D����״���£�22.4L����ϩ�к��еĹ��õ��Ӷ���Ϊ12 NA
|
3������� ��8�֣�����m gij���壬������˫ԭ�ӷ��ӹ��ɣ�����Ħ������ΪM g��mol-1���������ӵ���������ֵ��NA��ʾ����
��1������������ʵ���Ϊ?mol��?
��2������������ԭ������Ϊ?����
��3��������������1Lˮ�У������Ƿ�Ӧ��������Һ�����ʵ���������Ϊ?��
��4��������������1Lˮ��������Һ���ܶ�Ϊ�� g��cm-3�������ʵ���Ũ��Ϊ?mol/L��
4��ѡ���� ����ʱ�����������Ļ����Һ20mL������������μ���0.05mol/L Ba(OH)2��Һʱ�����ɵ�BaSO4��pH�ı仯��ͼ��ʾ����������Һ���ʱ����ı仯��������˵����ȷ����

A��ͼ��A����Һ��pH=1
B�����ɳ������������Ϊ2.33g
C��ԭ�����Һ���������ʵ���Ũ��Ϊ0.1mol/L
D����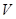 [Ba(OH)2(aq)]=10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++SO
[Ba(OH)2(aq)]=10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++SO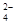 �TBaSO4��
�TBaSO4��
5��ʵ���� ��10�֣�ijͬѧ����ˮ�ʼ��վ����800mL 1 mol��L��1NaOH��Һ���á�
��1����ͬѧӦѡ��IJ������������ձ�����Ͳ������������ͷ�ι��⣬���� ��

��2���������������ͼ��ʾ������ͼ����Ӧ����ͼ�е� (��ѡ����ĸ)֮�䡣
A�������
B�������
C�������
D�������
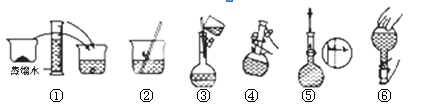
��3����ͬѧӦ��������ƽ��ȡNaOH���� g��������Ϊ33.1 g���ձ�����������ƽ�ϳ�ȡ����NaOH����ʱ��������ͼ��ѡ������ȷ��ʾ����λ�õ�ѡ�� ����ѡ����ĸ����
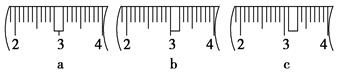
��4�����в�����������ҺŨ�ȴ�С�к�Ӱ�� (�ƫ����ƫС������Ӱ�족)��
�ٶ���ʱ�����Ӷ�����Ũ�Ȼ� ��
��ת����Һ�����У�δϴ�Ӳ��������ձ���Ũ�Ȼ� ��
������ƿδ���Ũ�Ȼ� ��
�ܶ���ҡ�Ⱥ�����Һ������ڿ̶��ߣ�������ˮ���̶��ߣ�Ũ�Ȼ� ��
��5��������Һ��ʵ�ʲ��������У�����Ҫ�죬�������� ����ʹ���Ƶ�NaOH��Һ��Ũ�ȱ�1 mol��L��1______�����С������

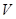 [Ba(OH)2(aq)]=10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++SO
[Ba(OH)2(aq)]=10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++SO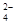 �TBaSO4��
�TBaSO4��

