| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ����ʵ��������⼼�ɣ�2019�����°棩(��)
�ο��𰸣�B ������������ʺ��ǵ�ԭ�ӷ��ӣ�����A���ڱ�״���µ������22.4L��B��64gSO2��1mol������3mol��ԭ�ӣ�B��ȷ�����³�ѹ�£�11.2L��������0.5mol��C����ȷ����״���£�ˮ�������壬��������������Ħ�������D����ȷ�������ȷ�Ĵ�ѡB�� �����Ѷȣ����� 2��ѡ���� ��ʾ�����ӵ�������������������ȷ���� |
�ο��𰸣�C
���������A����״�������ȼ�����Һ̬����������������Ħ�������A����B��1 mol FeI2������������Ӧ���������Ӻ͵�������ȫ����������ת�Ƶĵ�����Ϊ3NA��B����C�����ݵ���غ��֪c(Na��)+c(H��)��c(CH3COO��)+c(OH��)����Һ�����ԣ���c(H��)��c(OH��)������c(Na��)��c(CH3COO��)����Һ�������ӵ����ʵ�����1mol�������Һ��CH3COO����ĿΪNA��C��ȷ��D��������ϩ�ĵ���ʽ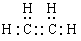 ��֪����ϩ���Ӻ���6�Ե��Ӷԣ����״���£�22.4L����ϩ�к��еĹ��õ��Ӷ���Ϊ6NA��D����ѡC��
��֪����ϩ���Ӻ���6�Ե��Ӷԣ����״���£�22.4L����ϩ�к��еĹ��õ��Ӷ���Ϊ6NA��D����ѡC��
���㣺���鰢��٤�������ļ������ж�
�����Ѷȣ�һ��
3������� ��8�֣�����m gij���壬������˫ԭ�ӷ��ӹ��ɣ�����Ħ������ΪM g��mol-1���������ӵ���������ֵ��NA��ʾ����
��1������������ʵ���Ϊ?mol��?
��2������������ԭ������Ϊ?����
��3��������������1Lˮ�У������Ƿ�Ӧ��������Һ�����ʵ���������Ϊ?��
��4��������������1Lˮ��������Һ���ܶ�Ϊ�� g��cm-3�������ʵ���Ũ��Ϊ?mol/L��
�ο��𰸣���1��m/M?��2��2 mNA/M?��3��m/��m��1000����100%?��4��1000��m/M��m+1000��
����������������ʵ������йؼ��㡣
��1������n��m/M��֪������������ʵ�����m/M mol��
��2������������2��ԭ�ӹ��ɵģ�����ԭ�ӵ����ʵ�����2m/M mol�����Ժ��е�ԭ��������2 mNA/M������
��3��1Lˮ������ˮ1000g�������Һ�������ǣ�1000��m��g���������ʵ�����������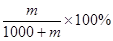 ��
��
��4����Һ�������ǣ�1000��m��g����Һ���ܶ��Ǧ� g��cm-3������Һ�������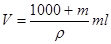 �����Ը���c��n/V��֪����Һ�����ʵ���Ũ����
�����Ը���c��n/V��֪����Һ�����ʵ���Ũ���� ��
��
�����Ѷȣ�һ��
4��ѡ���� ����ʱ�����������Ļ����Һ20mL������������μ���0.05mol/L Ba(OH)2��Һʱ�����ɵ�BaSO4��pH�ı仯��ͼ��ʾ����������Һ���ʱ����ı仯��������˵����ȷ����
A��ͼ��A����Һ��pH=1
B�����ɳ������������Ϊ2.33g
C��ԭ�����Һ���������ʵ���Ũ��Ϊ0.1mol/L
D���� [Ba(OH)2(aq)]=10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++SO
[Ba(OH)2(aq)]=10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++SO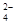 �TBaSO4��
�TBaSO4��
�ο��𰸣�A
�����������ͼ��֪��0��20mLBa(OH)2��Һ����H2SO4+Ba(OH)2�TBaSO4��+2H2O�����������ӷ���ʽ��2H����SO42��+Ba2����2OH���TBaSO4��+2H2O��D����20mL��60mLBa(OH)2��Һ��������H��+OH���TH2O����ͼ��֪������20mLBa(OH)2��Һʱ�����ᱵ���������ֵ������������ʵ���Ϊx����
H2SO4?+? Ba(OH)2?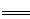 ?BaSO4��? +? H2O
?BaSO4��? +? H2O
1?1? 233g
x?0.02L��0.05mol��L��1? y
��x=0.02L��0.05mol��L��1=0.001mol��y��0.233g��
��������ʵ���Ũ��Ϊ ?=0.05mol��L��1���������ᱵ�������������Ϊ0.233g��B����
?=0.05mol��L��1���������ᱵ�������������Ϊ0.233g��B����
��ͼ��֪��PH=7ʱ������60mLBa(OH)2��Һ����H��+OH���TH2O��֪ԭ��Һ�к��е�n��H����=n��OH����=0.06L��0.05mol��L��1=0.003mol����n��HCl��=0.003mol��2��0.001mol��2=0.004mol��
��ԭ��Һ��HCl�����ʵ���Ũ��= ?=0.2mol��L��1��C����
?=0.2mol��L��1��C����
��ͼ��֪��A��������ȫ��Ӧ�������ӵ�Ũ��Ϊ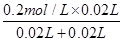 =0.1mol��L��1����pH=-lg0.1=1��A�ԣ�
=0.1mol��L��1����pH=-lg0.1=1��A�ԣ�
��������������ѡA��
�����Ѷȣ���
5��ʵ���� ��10�֣�ijͬѧ����ˮ�ʼ��վ����800mL 1 mol��L��1NaOH��Һ���á�
��1����ͬѧӦѡ��IJ������������ձ�����Ͳ������������ͷ�ι��⣬���� ��
��2���������������ͼ��ʾ������ͼ����Ӧ����ͼ�е� (��ѡ����ĸ)֮�䡣
A�������
B�������
C�������
D�������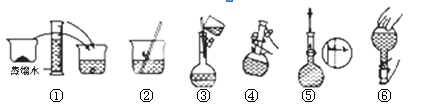
��3����ͬѧӦ��������ƽ��ȡNaOH���� g��������Ϊ33.1 g���ձ�����������ƽ�ϳ�ȡ����NaOH����ʱ��������ͼ��ѡ������ȷ��ʾ����λ�õ�ѡ�� ����ѡ����ĸ����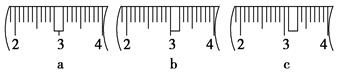
��4�����в�����������ҺŨ�ȴ�С�к�Ӱ�� (�ƫ����ƫС������Ӱ�족)��
�ٶ���ʱ�����Ӷ�����Ũ�Ȼ� ��
��ת����Һ�����У�δϴ�Ӳ��������ձ���Ũ�Ȼ� ��
������ƿδ���Ũ�Ȼ� ��
�ܶ���ҡ�Ⱥ�����Һ������ڿ̶��ߣ�������ˮ���̶��ߣ�Ũ�Ȼ� ��
��5��������Һ��ʵ�ʲ��������У�����Ҫ�죬�������� ����ʹ���Ƶ�NaOH��Һ��Ũ�ȱ�1 mol��L��1______�����С������
�ο��𰸣���1�� 1000mL����ƿ ��2�� D ��3�� 40.0 �� C ��4���� ƫС�� ƫС����Ӱ�� ��ƫС ��5�� �����еĶ�����̼����������Ʒ�Ӧ ��С
�����������1������һ�����ʵ���Ũ�ȵ���Һһ��Ҫ�õ�����ƿ������ƿ�Ĺ��û��800mL�ģ�����ѡ�������ϴ�ģ��ʻ�Ҫ1000mL����ƿ����2��ͼʾ�IJ����Ǽ�������ˮ���������������Һ֮��ҡ��֮ǰ����ѡD����3��ѡ��1000mL����ƿ�������Ƶ���Һ�����1000mL����n(NaOH)=cV=1 mol��L��1��1L=1.0mol��m(NaOH)=n��M=1.0mol��40g/mol=40.0g,����ʱ����Ӧ���Ƶ�3.1 g��λ�ô�����ʾ����λ����3.1 g������C����4���� ����ʱ�����Ӷ����������Һ���������Ũ�Ȼ�ƫС���� ת����Һ�����У�δϴ�Ӳ��������ձ����������������ʧ��Ũ�Ȼ�ƫС���������ƹ�������Ҫ��ˮ��������ƿδ�����Ũ����Ӱ�졣�� ����ҡ�Ⱥ�����Һ������ڿ̶��ߣ�������ˮ���̶��ߣ�������������Ũ�Ȼ�ƫС����5���������ƻ�������еĶ�����̼��Ӧ�����������������ʹ��һ�����������Ʒ�����Ӧ���������Ƶ���ҺŨ��ƫС��
���㣺һ�����ʵ���Ũ����Һ�����ơ�
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ���⡶���Ľṹ����Ƶ��.. | |
| �����Ŀ |