1、选择题 在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质
| X
| Y
| Z
|
初始浓度/mol・L-1
| 0.1
| 0.2
| 0
|
平衡浓度/mol・L-1
| 0.05
| 0.05
| 0.1
|
下列说法错误的是? (? )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
参考答案:C
本题解析:略
本题难度:一般
2、选择题 下图是温度和压强对X+Y 2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
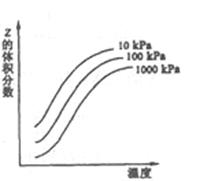
A.X、Y、Z均为气态
B.恒容时,混合气体的密度可作为此反应是否达到化学平衡[的判断依据
C.升高温度时 增大,
增大,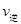 减小,平衡向右移动
减小,平衡向右移动
D.使用催化剂Z的产率增加
参考答案:B
本题解析:根据图像可知,随着温度的升高,生成物Z的含量逐渐升高,所以反应是吸热反应。但升高温度,正逆反应速率均是增加的,C不正确。当温度相同时,压强越大,生成物Z的含量越小,这说明增大压强,平衡向逆反应方向移动,说明正反应是体积增大的反应。若X、Y、Z均为气态,则反应前后气体的体积不变,A不正确。所以Z一定是气体,X和Y中只能有一种是气体。密度是混合气的质量和容器容积的比值,反应过程中质量是变化的,所以当密度不再发生变化时,可以说明反应达到平衡状态,C正确。催化剂不能改变平衡状态,D不正确。答案是B。
本题难度:一般
3、简答题 在一个固定容积的密闭容器中,保持一定温度,发生反应A(g)+B(g)?

?2C(g)?已知加入1mol?A和2molB,在达到平衡后生成了amolC,此时C在平衡混合物中的体积分数为M%.在相同实验条件下,
(1)若往相同容器中加入2molA?4molB,平衡后C的物质的量为______mol.
(2)若往相同容器中加入0.5molC,若要求平衡后C的物质的量为0.5a?mol.平衡后C的体积分数仍为M%,则还应往容器中加入A______mol,B______mol.
(3)若往相同容器中加入2molA、6molB,若要求平衡后C的体积分数仍为M%,则应加入C______mol,平衡后C的物质的量为______mol.
参考答案:(1)恒温恒容下,改为加入2molA和4molB,A、B的物质的量之比为1:2,与原平衡相同,反应为前后气体体积不变,所以与原平衡等效,转化率不变,各组分含量不变,C的体积分数为M%=a3,所以C的物质的量为a3×(2mol+4mol)=2amol,
故答案为:2amol
(2)平衡后C在反应混合气中的体积分数不变,两平衡等效,反应为前后气体体积不变的反应,按化学计量数转化到左边,应满足A、B的物质的量之比为1:2.平衡后C的物质的量为0.5a?mol,由于C的体积分数为a3,所以平衡后反应混合物总物质的量为1.5mol.
令还应加入A的物质的量为xmol,加入B的物质的量为ymol,则:(0.25+x)mol:(0.25+y)mol=1:2,且0.5+x+y=1.5
解得x=0.25,y=0.75.
故答案为:0.25;0.75
(3)衡后C在反应混合气中的体积分数不变,两平衡等效,反应为前后气体体积不变的反应,按化学计量数转化到左边,应满足A、B的物质的量之比为1:2.令还应加入C的物质的量为nmol,则:(2+0.5n)mol:(6+0.5n)mol=1:2,
解得n=4.
平衡后C的物质的量为a3×(2+6+4)mol=4amol
故答案为:4;4a
本题解析:
本题难度:一般
4、选择题 在一定温度下、一定体积条件下,能说明下列反应达到平衡状态的是(?)
A.反应2SO2(g)+O2(g) 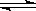 2SO3(g) 容器内的密度不随时间变化
2SO3(g) 容器内的密度不随时间变化
B.反应A2(g)+B2(g) 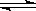 2AB(g)容器内的总压强不随时间变化
2AB(g)容器内的总压强不随时间变化
C.反应N2+3H2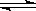 2NH3容器内气体平均相对分子质量不随时间变化
2NH3容器内气体平均相对分子质量不随时间变化
D.反应4A(s)+3B(g)  2C(g)+D(g)容器内气体平均相对分子质量不随时间变化
2C(g)+D(g)容器内气体平均相对分子质量不随时间变化
参考答案:CD
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。密度是混合气的质量和容器容积的比值,A中在反应过程中质量和容积始终是不变的,不能说明;B中反应前后气体体积是不变的,所以压强也是始终不变的,B不正确;混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,C中质量不变,但物质的量是变化的,而D中物质的量不变,但气体的质量是变化的,所以都可以说明,答案选CD。
点评:判断化学平衡状态的标志有:(1)任何情况下均可作为标志的:①υ正=υ逆(同一种物质);②各组分含量(百分含量、物质的量、质量)不随时间变化;③某反应物的消耗(生成)速率、某生成物的消耗(生成)速率=化学计量数之比;(2)在一定条件下可作为标志的是:①对于有色物质参加或生成的可逆反应体系,颜色不再变化;②对于有气态物质参加或生成的可逆反应体系,若反应前后气体的系数和相等,则混合气体平均相对分子质量M和反应总压P不变(恒温恒容);③对于恒温绝热体系,体系的温度不在变化;(3)不能作为判断标志的是:①各物质的物质的量或浓度变化或反应速率之比=化学计量数之比 (任何情况下均适用);②有气态物质参加或生成的反应,若反应前后气体的系数和相等,则混合气体平均相对分子质量M和反应总压P不变(恒温恒容)。
本题难度:一般
5、填空题 (16分)完成下列各题:
⑴K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车。
①若司机酒后开车,检测仪器内物质显示出?色。
②写出并配平该反应的化学方程式:?。
③如果在反应中生成1mol氧化产物,转移的电子总数为?。
⑵在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g)+ O2(g)="2NO(g)?" △H=+180. 5 kJ/mol?
5 kJ/mol?
2C(s)+ O2(g)="2CO(g)?" △H=-221.0 kJ/mol
C(s)+ O2(g)=CO2(g)? △H=-393.5 kJ/mol
①尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)? △H =?。
②为了提高尾气转化的反应的速率和NO的转化率,采取的正确措施为?。
A.加催化剂同时升高温度
B.加催化剂同时增大压强
C.升高温度同时充入N2
D.降低温度同时增大压强
 ?。(填序号)
?。(填序号)