1、选择题 下图是反应A2(g)+3B2(g)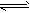 2C(g)△H<0 的平衡移动图,影响该反应平衡移动的原因是
2C(g)△H<0 的平衡移动图,影响该反应平衡移动的原因是
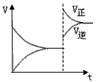
[? ]
A.升高温度
B.增大反应物浓度
C.增大压强
D.使用催化剂
2、选择题 对可逆反应4NH3(g)+5O2(g)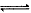 4NO(g)+6H2O(g)下列叙述正确的是
4NO(g)+6H2O(g)下列叙述正确的是
[? ]
A.达到化学平衡时,4v正(O2) =5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3) =3v正(H2O)
3、选择题 将2mol?SO2,1mol?O2?充入带活塞的密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g),达到平衡后,改变下列条件,SO3的平衡浓度不改变的是( )
A.保持温度和容器的压强不变,充入1mol?SO3(g)
B.保持温度和容器的容积不变,充入1mol?SO3(g)
C.保持温度和容器的压强不变,充入1mol?O2(g)
D.保持温度和容器的压强不变,充入1mol?Ar
4、选择题 对于平衡CO2(g)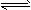 CO2(aq) ΔH=-19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是
CO2(aq) ΔH=-19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是
[? ]
A.升温增压
B.降温减压
C.升温减压
D.降温增压
5、填空题 工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2?(g)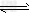 2SO3(g)?△H=-196.6?kJ・mol-1
2SO3(g)?△H=-196.6?kJ・mol-1
⑴生产中为提高反应速率和SO2的转化率,下列措施可行的是_______(填字母,下同)。
A.向装置中充入N2?
B.向装置中充入过量的SO2
C.向装置中充入O2?
D.升高温度
⑵若在一定温度下,向一个容积可变的恒压容器中,通入3mol?SO2?和2mol?O2?及固体催化剂,发生上述反应,平衡时容器内气体体积为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为?5mol?SO2(g)、3.5?mol?O2(g)、1mol?SO3(g)?,下列说法正确的是___________
A.第一次平衡时反应放出的热量为294.9kJ?
B.两次平衡SO2的转化率相等
C.两次平衡时的O2体积分数相等?
D.第二次平衡时SO3的体积分数等于2/9
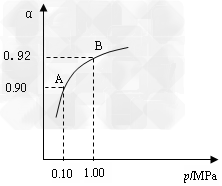
⑶生产中在550?℃时,将2.0?mol?SO2和1.0?mol?O2置于 5?L密闭容器中,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图所示。反应达平衡后,体系总压强为
0.10?M?Pa。试计算反应 2SO3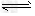 2SO2+O2?在550?℃时的平衡常数K=_________。 A、B表示不同压强下的平衡转化率,通常工业生产中采用常压的原因是:__________________,并比较不同压强下的平衡常数:K(0.10?MPa)?_________K(1.0?MPa)(填?“<”或“>”或“=”)。
2SO2+O2?在550?℃时的平衡常数K=_________。 A、B表示不同压强下的平衡转化率,通常工业生产中采用常压的原因是:__________________,并比较不同压强下的平衡常数:K(0.10?MPa)?_________K(1.0?MPa)(填?“<”或“>”或“=”)。
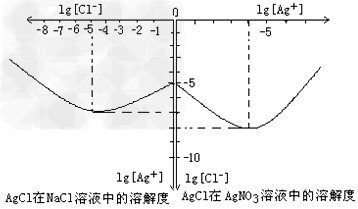
⑷沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。已知AgCl?+?Cl-?=[AgCl2]-,下图是某温度下AgCl在NaCl溶液中的溶解情况。由以上信息可知:
①由图知该温度下AgCl的溶度积常数为__________________________。
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:__________________________?