1ЎўСЎФсМв ТСЦӘ298KКұ·ҙУҰ2SO2ЈЁgЈ©+O2ЈЁgЈ©ЁT2SO3ЈЁgЈ©ЎчH=-197kJ?mol-1Ј¬ФЪПаН¬ОВ¶ИПВПтТ»ГЬұХИЭЖчЦРјУИл2molSO2әН1molO2Ј¬ҙп»ҜС§ЖҪәвКұ·ЕіцИИБҝОӘa1kJЈ»ПтБнТ»ИЭ»эПаН¬өДГЬұХИЭЖчЦРНЁИл1molSO2әН0.5molO2Ј¬ҙп»ҜС§ЖҪәвКұ·ЕіцИИБҝОӘa2kJЈ¬ФтПВБР№ШПөКҪЦРХэИ·өДКЗЈЁЎЎЎЎЈ©
AЈ®2a2Јҫa1Јҫ197
BЈ®2a2Јјa1Јј197
CЈ®2a2=a1Јҫ197
DЈ®2a2=a1=197
2ЎўМоҝХМв ·ҙУҰ2A BЈ«CЈ¬ФЪДіТ»ОВ¶ИКұЈ¬ҙпөҪЖҪәв
BЈ«CЈ¬ФЪДіТ»ОВ¶ИКұЈ¬ҙпөҪЖҪәв
ЈЁ1Ј©ИфОВ¶ИЙэёЯЈ¬»ҜС§ЖҪәвіЈКэұдРЎЈ¬ФтХэ·ҙУҰКЗ_____ИИ·ҙУҰЎЈ
ЈЁ2Ј©ИфBКЗ№ММеЈ¬ҪөөНС№ЗҝКұЈ¬ЖҪәвПтЧуТЖ¶ҜЈ¬ФтAКЗ_____М¬ЎЈ
ЈЁ3Ј©ИфAКЗЖшМ¬Ј¬јУС№КұЈ¬ЖҪәвІ»ТЖ¶ҜЈ¬ФтBОӘ_____М¬Ј¬CОӘ____М¬ЎЈ
3ЎўМоҝХМв Т»¶ЁМхјюПВЈ¬ФЪМе»эОӘ3 LөДГЬұХИЭЖчЦРЈ¬Т»Сх»ҜМјУлЗвЖш·ҙУҰЙъіЙјЧҙј(ҙЯ»ҜјБОӘCu2O/ZnO)Јә
CO(g)Ј«2H2(g)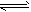 CH3OH(g)
CH3OH(g)
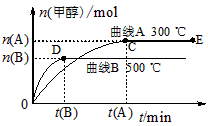
ёщҫЭМвТвНкіЙПВБРёчМвЈә
(1)·ҙУҰҙпөҪЖҪәвКұЈ¬ЖҪәвіЈКэұнҙпКҪKЈҪ_________Ј¬ЙэёЯОВ¶ИЈ¬KЦө_________ (МоЎ°ФцҙуЎұЎўЎ°јхРЎЎұ»тЎ°І»ұдЎұ)ЎЈ
(2)ФЪ500 ЎжЈ¬ҙУ·ҙУҰҝӘКјөҪЖҪәвЈ¬ЗвЖшөДЖҪҫщ·ҙУҰЛЩВКv (H2)ЈҪ_________ЎЈ
(3)ФЪЖдЛыМхјюІ»ұдөДЗйҝцПВЈ¬¶ФҙҰУЪEөгөДМеПөМе»эС№ЛхөҪФӯАҙөД1/2Ј¬ПВБРУР№ШёГМеПөөДЛө·ЁХэИ·өДКЗ
_________
aЈ®ЗвЖшөДЕЁ¶ИјхЙЩ
bЈ®Хэ·ҙУҰЛЩВКјУҝмЈ¬Дж·ҙУҰЛЩВКТІјУҝм
cЈ®јЧҙјөДОпЦКөДБҝФцјУ
dЈ®ЦШРВЖҪәвКұn(H2)/n(CH3OH)Фцҙу
(4)ҫЭСРҫҝЈ¬·ҙУҰ№эіМЦРЖрҙЯ»ҜЧчУГөДОӘCu2OЈ¬·ҙУҰМеПөЦРә¬ЙЩБҝCO2УРАыУЪО¬іЦҙЯ»ҜјБCu2OөДБҝІ»ұдЈ¬ФӯТтКЗЈә_____________________(УГ»ҜС§·ҪіМКҪұнКҫ)ЎЈ
4ЎўМоҝХМв УРБҪЦ»ГЬұХИЭЖчAәНBЈ¬AДЬұЈіЦәгС№Ј¬BДЬұЈіЦәгИЭЎЈЖрКјКұПтИЭ»эПаөИөДAЎўBЦР·ЦұрНЁИлМе»эұИОӘ2ЎГ1өДөИБҝөДSO2әНO2Ј¬К№Ц®·ўЙъ·ҙУҰЈә2SO2+O2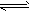 2SO3Ј¬ІўҙпөҪЖҪәвЎЈФтЈЁМо>Ўў=Ўў<Ј»ЧуЎўУТЈ»ФцҙуЎўјхРЎЎўІ»ұдЈ©ЎЈ
2SO3Ј¬ІўҙпөҪЖҪәвЎЈФтЈЁМо>Ўў=Ўў<Ј»ЧуЎўУТЈ»ФцҙуЎўјхРЎЎўІ»ұдЈ©ЎЈ
ЈЁ1Ј©ҙпөҪЖҪәвЛщРиТӘөДКұјдЈәt(A)_________t(B)Ј¬SO2өДЧӘ»ҜВКЈәa(A)_________a(B)
ЈЁ2Ј©ЖрКјКұБҪИЭЖчЦРөД·ҙУҰЛЩВКЈәv(A)_________v(B)Ј¬·ҙУҰ№эіМЦРөД·ҙУҰЛЩВКЈәv(A)_________v(B)ЎЈ
ЈЁ3Ј©ҙпөҪЖҪәвКұЈ¬ФЪБҪИЭЖчЦР·ЦұрНЁИлөИБҝөДAVЖшЎЈAЦРөД»ҜС§ЖҪәвПт ·ҙУҰ·ҪПтТЖ¶ҜЈ¬BЦРөД»ҜС§·ҙУҰЛЩВК__________________ЎЈ
ЈЁ4Ј©ҙпөҪЖҪәвәуЈ¬ПтБҪИЭЖчЦР·ЦұрНЁИлөИБҝөДФӯ·ҙУҰЖшМеЈ¬ФЩҙОҙпөҪЖҪәвКұЈ¬AИЭЖчЦРSO2өД°Щ·Цә¬Бҝ
_________Ј¬BИЭЖчЦРSO2өД°Щ·Цә¬Бҝ_________ЎЈ
5ЎўСЎФсМв Т»¶ЁМхјюПВЈ¬Ме»эОӘ10LөДГЬұХИЭЖчЦРЈ¬2molXәН1molYҪшРР·ҙУҰЈә2XЈЁgЈ©+YЈЁgЈ© ZЈЁgЈ©Ј¬ҫӯ60sҙпөҪЖҪәвЈ¬ЙъіЙ0.3molZЎЈПВБРЛө·ЁХэИ·өДКЗ
ZЈЁgЈ©Ј¬ҫӯ60sҙпөҪЖҪәвЈ¬ЙъіЙ0.3molZЎЈПВБРЛө·ЁХэИ·өДКЗ
[? ]
AЈ®ТФYұнКҫөД·ҙУҰЛЩВКОӘ0.001molЎӨL-1ЎӨs-1
BЈ®Ҫ«ИЭЖчМе»эұдОӘ20LЈ¬ZөДЖҪәвЕЁ¶ИұдОӘФӯАҙөД1/2
CЈ®ИфФЪёГИЭЖчЦРФЩНЁИл2molXәН1molYЈ¬ФтОпЦКYөДЧӘ»ҜВКјхРЎ
DЈ®ИфЙэёЯОВ¶ИЈ¬XөДМе»э·ЦКэФцҙуЈ¬ФтёГ·ҙУҰөДЎчH<0