1、填空题 往20mL硫酸和盐酸的混合溶液中,加入0.05mol/LBa(OH)2溶液时,生成BaSO4的量和溶液的pH变化如右图。试回答:
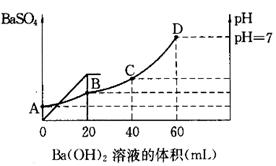
(1)起始时,混酸中H2SO4的物质的量浓度为?
(2)起始时,混酸中盐酸的物质的量浓度为?
(3)B点时溶液的pH是?。
参考答案:(1)0.05mol/L?(2)0.2mol/L?(3)1
本题解析:(1)根据图像可知,当加入20ml氢氧化钡时,沉淀达到最大值,所以硫酸的物质的量是0.02L×0.05mol/L=0.001mol,则硫酸的浓度是0.001mol÷0.02L=0.05mol/L。
(2)当Ph=7是,酸碱恰好中和,则盐酸的物质的量是2×0.04L×0.05mol/L=0.004mol,则盐酸的浓度是0.004mol÷0.02L=0.2mol/L。
(3)B点相当于是硫酸被中和,则溶液中氢离子的浓度是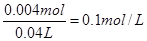 ,所以pH=1。
,所以pH=1。
点评:该题是基础性试题的考查,试题基础性强,侧重对学生基础知识的巩固和训练。旨在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确图像的变化趋势特点,然后结合题意灵活运用即可。
本题难度:一般
2、选择题 关于常温下pH=2的醋酸溶液,下列叙述正确的是
A.c(CH3COOH)=0.01mol・L-1
B.c(H+)=c(CH3COO-)
C.加水稀释100倍后,溶液pH=4
D.醋酸的电离常数为Ka,CH3COO-的水解常数为Kh,则Ka・Kh=Kw
参考答案:D
本题解析:醋酸部分电离,它的起始物质的量浓度比c(H+)大得多,A错;由于水也电离出H+,c(H+)>c(CH3COO-)B错;加水稀释100倍,pH上升不到2个单位,C错。Kh=c(OH-)(CH3COOH)/c(CH3COO-),给表达式上下同乘以c(H+),方可推断出Ka・Kh=Kw。答案选D。
本题难度:一般
3、选择题 下列化学式表示的粒子对H2O的电离平衡不产生影响的是
A.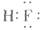
B.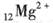
C.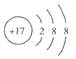
D.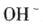
参考答案:C
本题解析:水是一种弱电解质,存在电离平衡,方程式为H2O H++OH-。所以酸或碱能抑制水的电离,而发生水解的某些盐促进水的电离,A、D抑制水的电离,镁离子水解促进水的电离,氯离子既不能促进也不能抑制水的电离,答案选C。
H++OH-。所以酸或碱能抑制水的电离,而发生水解的某些盐促进水的电离,A、D抑制水的电离,镁离子水解促进水的电离,氯离子既不能促进也不能抑制水的电离,答案选C。
本题难度:一般
4、选择题 下列溶液中微粒浓度关系一定正确的是( )
A.氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+)
B.新制氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.室温下,向0.01 mol・L-1 NH4HSO4溶液中滴加等浓度等体积的NaOH溶液:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
D.pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+)
参考答案:C
本题解析:溶液呈中性,溶液中氢离子和氢氧根离子浓度相等,所以溶液中氯离子浓度和铵根离子浓度相等,故A错误;新制氯水溶液呈酸性,所以氢离子浓度大于氢氧根离子浓度,次氯酸电离氢离子、氯化氢电离出氢离子导致氢离子浓度大于氯离子浓度,故B错误;当酸为强酸时,溶液呈中性,氢离子浓度等于氢氧根离子浓度;当酸为弱酸时,酸的浓度大于碱的浓度,所以溶液呈酸性,氢离子浓度大于氢氧根离子浓度,故D错误。
本题难度:一般
5、选择题 某溶液中含有SO32-、SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断正确的是
①反应前后,溶液中离子浓度基本保持不变的只有Na+?②有胶状物质生成?③有气体产生?
④溶液颜色发生变化?⑤共发生了2个氧化还原反应
A.①②③④⑤
B.①②③④
C.①③⑤
D.②④⑤
参考答案:A
本题解析:略
本题难度:一般