1、选择题 低脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0在恒容的密闭容器中,下列有关说法正确的是( )
A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C.单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
参考答案:A、放热反应升温,平衡向逆反应方向移动,平衡常数减小,故A错误;
B、增大一个反应物浓度另一反应物转化率增大,故B错误;
C、单位时间内消耗NO和N2的物质的量比为1:2时,正逆反应速率相等,故C正确.
D、使用催化剂平衡不移动,故D错误.
故选C.
本题解析:
本题难度:一般
2、选择题 可逆反应H2(g)+I2(g)?

2HI(g)达到平衡状态时的标志是( )
A.混合气体的体积恒定不变
B.混合气体的颜色不再改变
C.H2,I2,HI的浓度相等
D.I2的生产速率等于H2的生产速率
参考答案:A、该反应是反应前后气体体积不变的化学反应,所以无论反应是否达到平衡状态混合气体的体积始终恒定不变,故A错误;
B、该反应中碘有颜色,其他物质无颜色,当反应达到平衡状态时,各种物质的物质的量、浓度等不再发生变化,所以混合气体的颜色不再改变,故B正确;
C、平衡时,各物质的浓度与反应的初始浓度、转化率有关,所以H2、I2、HI的浓度相等不是化学平衡状态的标志,故C错误;
D、只要有逆反应发生,无论该反应是否达到平衡状态,I2的生成速率始终等于H2的生成速率,故D错误;
故选B.
本题解析:
本题难度:简单
3、选择题 可逆反应在一定条件下达到化学平衡状态的标志是( )
A.反应停止了?
B.正反应速率与逆反应速率相等均为零
C.反应物和生成物浓度相等?
D.反应物和生成物浓度不再变化
参考答案:A.化学反应为动态平衡,达到平衡状态时,正逆反应速率相等,但反应没有停止,故A错误;
B.达到平衡状态时,正逆反应速率相等,但不等于零,故B错误;
C.达到平衡状态时,反应物和生成物浓度关系不能确定,取决于起始物质的量浓度以及反应转化程度,不能作为判断是否达到平衡状态的依据,故C错误;
D.当反应物和生成物浓度不再变化时,达到平衡状态,故D正确.
故选D.
本题解析:
本题难度:一般
4、选择题 对于可逆反应A(g) + 2B(g) 2C(g)(正反应吸热),下列图象正确的是
2C(g)(正反应吸热),下列图象正确的是
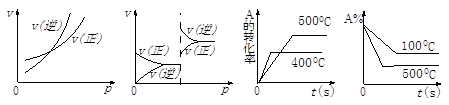
A? B? C? D
参考答案:D
本题解析:A、该反应是一个反应前后体积不变的反应,因此增大压强对正逆反应来讲是同等程度的改变大小,错误;B、错误跟A的原因一样;C、应该遵守“先拐先平,数值大”,错误;D、正确。
本题难度:一般
5、选择题 下列描述违背化学原理的是(? )
A.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
B.反应A(g)+3B(g) 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
C.SO2的催化氧化是一个放热的反应,升高温度,反应速率加快
D.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-= Cl2 ↑
参考答案:B
本题解析:平衡常数只与温度有关,所以增大压强,不论平衡如何移动,平衡常数均不变。答案选B。
本题难度:简单