1、填空题 在某一容积为5 L的密闭容器内,加入 0.3 mol的CO和0.3 mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g)?ΔH>0,反应中CO2的浓度随时间变化情况如图:
CO2(g)+H2(g)?ΔH>0,反应中CO2的浓度随时间变化情况如图:
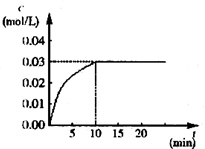
(1)根据图上数据,反应开始至达到平衡时,CO的化学反应速率为v(CO)=?mol/(L・min)-1,该温度下的平衡常数K=?。
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有?(填字母)
A升高温度;B降低温度;C增大压强;D减小压强;E加入催化剂;G移出一氧化碳气体
(3)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.2 mol的CO2和0.2 mol的H2,在相同的条件下,反应达平衡时,c(CO)=?mol/L。
(4)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol 的水蒸气,重新达到平衡后,CO的转化率?(填“升高”、“降低”还是“不变”),CO2的质量分数?(填“升高”、“降低”还是“不变”)。
(5)在催化剂存在和800℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09mol/L,c(CO2)=c(H2)=0.13mol/L,则此反应是否处于平衡状态?(填“是”或“否”),若没有处于平衡状态则该反应向?移动。(填“正方向”或“逆方向”)
参考答案:(1)0.003? 1?(2)A?(3)0.003?(4)升高?降低?(5)否?逆方向
本题解析:(1)根据图像可知,反应进行到10min是达到平衡状态。此时生成的CO2的物质的量浓度是0.03mol/L,则根据方程式可知消耗CO的浓度是0.03mol/L,因此CO的化学反应速率为v(CO)=0.03mol/L÷10min=0.003mol/(L・min)-1。根据方程式可知
CO(g)+H2O(g)  ?CO2(g)+H2(g)
?CO2(g)+H2(g)
起始浓度(mol/L)? 0.06? 0.06? 0? 0
转化浓度(mol/L)? 0.03? 0.03? 0.03? 0.03
平衡浓度(mol/L)? 0.03? 0.03? 0.03? 0.03
所以该温度下反应的平衡常数K=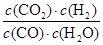 =1
=1
(2)平衡常数只与温度有关系,与平衡移动变为直接关系,因此选项CDEG中平衡常数均是不变的。正方应是吸热反应,升高温度平衡向正反应方向移动,平衡常数增大。反之降低温度平衡常数减小,因此答案选A。
(3)? CO(g)+H2O(g)  ?CO2(g)+H2(g)
?CO2(g)+H2(g)
起始浓度(mol/L)? 0.02? 0.02? 0.04? 0.04
转化浓度(mol/L)? x? x? x? x
平衡浓度(mol/L)0.02-x? 0.02-x? 0.04+x? 0.04+x
则根据反应的平衡常数K=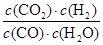 =1可知
=1可知
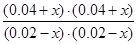 =1
=1
解得x=-0.01
所以平衡时CO的浓度是0.03mol/L
(4)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol 的水蒸气,水蒸气的浓度增大,平衡向正反应方向移动。所以重新达到平衡后,CO的转化率升高,根据方程式可知
CO(g)+H2O(g)  ?CO2(g)+H2(g)
?CO2(g)+H2(g)
起始浓度(mol/L)? 0.06? 0.12? 0? 0
转化浓度(mol/L)? x? x? x? x
平衡浓度(mol/L) 0.06-x? 0.12-x? x? x
则根据反应的平衡常数K=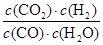 =1可知
=1可知
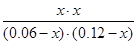 =1
=1
解得x=0.04
所以CO2的质量分数=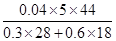 ×100%=45.83%
×100%=45.83%
而未加入之前CO2的质量分数=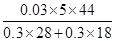 ×100%=47.83%
×100%=47.83%
所以CO2的质量分数减小
(5)在某一时刻测得c(CO)=c(H2O)=0.09mol/L,c(CO2)=c(H2)=0.13mol/L,则根据平衡常数表达式K=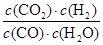 可知,此时
可知,此时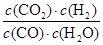 >1,所以反应没有达到平衡状态,该反应向逆反应方向移动。
>1,所以反应没有达到平衡状态,该反应向逆反应方向移动。
本题难度:一般
2、选择题 一定温度下,可逆反应3X(g)+Y(g)
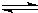
2Z(g)达到限度的标志是( )
A.单位时间内生成3nmolX,同时消耗nmolY
B.X、Y、Z的浓度相等
C.X的生成速率与Z的生成速率相等
D.X、Y、Z的分子个数比为3:1:2
参考答案:A.单位时间内生成3nmolX,同时消耗nmolY,可说明正逆反应速率相等,达到平衡状态,故A正确;
B.平衡时各物质的浓度取决于反应开始时的配料比以及反应转化的程度,不能用来判断是否达到平衡状态,故B错误;
C.X的生成速率与Z的生成速率相等,则正逆反应速率不等,没有达到平衡状态,故C错误;
D.平衡时各物质的分子数关系取决于反应起始物质的量以及转化的程度,不能用来判断是否达到平衡状态,故D错误.
故选A.
本题解析:
本题难度:一般
3、填空题 氮化硅(Si3N4)是一种新型陶瓷材料,它可在高温下的氮气流中由石英与焦炭通过以下反应制得:3SiO2(s) + 6C(s) + 2N2(g) Si3N4(s) + 6CO(g) + Q(Q>0)
Si3N4(s) + 6CO(g) + Q(Q>0)
完成下列填空:
(1)某温度下该反应在一容积为2L的密闭容器中进行,2min后达到平衡,刚好有2mol电子发生转移,则2min内反应的速率为:v(CO) = ?;该反应的平衡常数表达式为 ?。
(2)其它条件不变时仅增大压强,则?。
a.K值减小,平衡向逆反应方向移动?
b.K值增大,平衡向正反应方向移动
c.K值不变,平衡向逆反应方向移动?
d.K值不变,平衡向正反应方向移动
(3)一定条件下能说明上述反应已达平衡的是 ?。
a.c(N2 ) : c(CO) = 1:3? b.3v(N2 ) = v(CO)
c.固体质量不再改变? d.气体密度不再改变
达到平衡后改变某一条件,反应速率v与时间t的关系如图所示。?
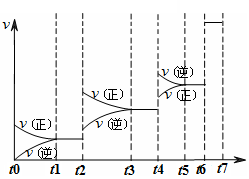
若不改变N2与CO的量,则图中t4时引起变化的原因可能是 ?;图中t6时引起变化的原因可能是?。
由图可知,平衡混合物中CO含量最高的时间段是?。
参考答案:(1)0.25mol/L・min(1分,计算或单位错不给分);?K=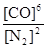 (1分)(2)c?(1分)
(1分)(2)c?(1分)
(3)c、d(1分×2)33、升高温度或缩小体积(增大压强)(1分);加入了催化剂(1分)。
t3~t4(1分)。
本题解析:(1)可逆反应3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)的平衡常数k=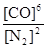 该反应为放热反应,升高温度平衡逆反应进行,化学平衡常数减小;(2)由方程式可知,该反应正反应是气体物质的量增大的反应,混乱度增大,熵值增大,故△S>0;故答案为:>;(3)A.单位时间生成2摩尔Si3N4的同时生成1摩尔的N2,生成2摩尔Si3N4的消耗4molN2,氮气的生成速率与消耗速率不相等,反应未达平衡状态,故A错误;B.平衡时c(N2)与c(CO)之比为1:3,可能处于平衡状态,也可能不处于平衡状态,与氮气的转化率等有关,故B错误;C.平衡时平衡体系个组分的含量不变,CO的百分含量 保持不变,说明到达平衡状态,故C正确;D.单位时间消耗1摩尔SiO2的同时生成2摩尔的C,消耗1摩尔SiO2需要消耗2molC,C的生成速率与消耗速率相等,反应达平衡状态,故D正确;故选CD;(4)若不改变N2、CO的量,由图可知,t4时瞬间正、逆反应都增大,平衡向逆反应移动,改变条件为升高温度后压缩体积增大压强;t6时瞬间正、逆反应都增大,平衡不移动,故应是加入催化剂;t2时改变改变条件,平衡向正反应移动,在t3时重新到达平衡,t4时改变条件,平衡向逆反应移动,t5时由达平衡,故t3~t4平衡状态CO的含量最高;故答案为:升高温度后压缩体积增大压强;加入催化剂;t3~t4。
该反应为放热反应,升高温度平衡逆反应进行,化学平衡常数减小;(2)由方程式可知,该反应正反应是气体物质的量增大的反应,混乱度增大,熵值增大,故△S>0;故答案为:>;(3)A.单位时间生成2摩尔Si3N4的同时生成1摩尔的N2,生成2摩尔Si3N4的消耗4molN2,氮气的生成速率与消耗速率不相等,反应未达平衡状态,故A错误;B.平衡时c(N2)与c(CO)之比为1:3,可能处于平衡状态,也可能不处于平衡状态,与氮气的转化率等有关,故B错误;C.平衡时平衡体系个组分的含量不变,CO的百分含量 保持不变,说明到达平衡状态,故C正确;D.单位时间消耗1摩尔SiO2的同时生成2摩尔的C,消耗1摩尔SiO2需要消耗2molC,C的生成速率与消耗速率相等,反应达平衡状态,故D正确;故选CD;(4)若不改变N2、CO的量,由图可知,t4时瞬间正、逆反应都增大,平衡向逆反应移动,改变条件为升高温度后压缩体积增大压强;t6时瞬间正、逆反应都增大,平衡不移动,故应是加入催化剂;t2时改变改变条件,平衡向正反应移动,在t3时重新到达平衡,t4时改变条件,平衡向逆反应移动,t5时由达平衡,故t3~t4平衡状态CO的含量最高;故答案为:升高温度后压缩体积增大压强;加入催化剂;t3~t4。
本题难度:困难
4、选择题 下列说法正确的是 ( )
①活化分子间的碰撞一定能发生化学反应
②普通分子有时也能发生有效碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应实质是活化分子有合适取向时的有效碰撞
A.③④⑥
B.①②⑤
C.③④⑤⑥
D.②③④
参考答案:A
本题解析:活化分子间的碰撞不一定能发生化学反应,①错误;只有活化分子才能发生有效碰撞,②错误;使用催化剂能提高反应速率,原因是催化剂可以降低反应的活化能,使有效碰撞频率增大,⑤错误,其余选项都是正确的,答案选A。
点评:该题是中等难度试题的考查,侧重考查学生对活化分子、有效碰撞等有关概念的熟悉了解程度,以及灵活运用基础知识解决实际问题的能力,有利于调动学生的学习兴趣和学习积极性。
本题难度:简单
5、填空题 (7分)某容积和温度不变的容器中,发生下列反应:
A(g)+2B(g) 2C(g)(正反应放热)
2C(g)(正反应放热)
回答下列问题:
(1)从A、B两气体充入容器至反应达到平衡状态,在此过程中,容器内压强____________(填“变大”“变小”或“不变”,下同),达到平衡后容器内压强___________________。
(2)使平衡体系的体积缩小,则气体A的浓度____________,气体C的物质的量___________________。
(3)化学反应达平衡状态后,加入适量的催化剂,则气体A的物质的量____________。
(4)若在平衡体系中,再充入一些气体A,则A的浓度____________,A的转化率________________________。
参考答案:(1)变小?不变?(2)变大?变大?(3)不变?(4)变大?变小
本题解析:(1)正反应是气体体积缩小的反应,开始到平衡的过程中,气体压强逐渐变小,达到平衡后,容器内气体的物质的量不变,气体的压强也不变。
(2)体积缩小,气体的压强变大,平衡向右移动以减弱压强的增加,但不能减弱到原来的程度,故新平衡建立时A的浓度比原平衡还是变大了;平衡向右移动,C的物质的量变大。
(3)加入催化剂,平衡不移动,A的物质的量不变。
(4)恒容下充入A,A的浓度变大,平衡向右移动,A的转化率变小,因为虽然转化的A增多了,但A的总物质的量也比原来大,且后者增率更大。
本题难度:简单