1、选择题 已知在某条件下O2的密度为1.28 g・L-1。在实验室用KClO3制O2,生成O2的平均速率为0.01 mol・L-1・min-1,则要制取500 mL O2,需要的时间为(?)
A.1 min
B.2 min
C.3 min
D.4 min
2、选择题 下列说法中可以充分说明反应:P(气)+Q(气)?R(气)+S(气),在该温度下已达平衡状态的是( )
A.反应容器内压强不随时间变化
B.P和S的生成速率相等
C.反应容器内P、Q、R、S四者共存
D.反应容器内总物质的量不随时间而变化
3、填空题 (14分)二甲醚(CH3OCH。)和甲醇(CH3OH)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
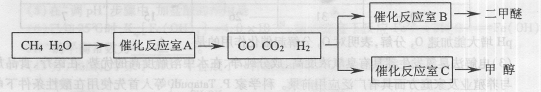
(1)催化反应室B中CO 与H2合成二甲醚的化学方程式为?.
与H2合成二甲醚的化学方程式为?.
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g) CO(g)+3H2(g)……(I)、CO(g)+H2O(g)
CO(g)+3H2(g)……(I)、CO(g)+H2O(g) CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g) CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g)
CH3OH(g)……(Ⅲ)、CO2(g)+3H2(g) CH3OH(g)+H2O(g)……(Ⅳ)
CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率= ×100%,试求反应(Ⅳ)的原子利用率为?。
×100%,试求反应(Ⅳ)的原子利用率为?。
②反应(Ⅳ)的△S ?0(填“>”、“=”或“<”)。
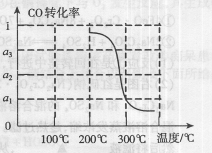
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如右图。则该反应的△H?0(填“>”、“=”或“<”)。300℃时该反应的平衡常数K= ?(用含字母的代数式表示)。
(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:
CH3OCH3一12e一+16OH一=2CO2-3+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
①将含SO2的废气通人电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回 收。
收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量。
4、选择题 恒温、恒压下,1molA和nmolB在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成
amolC,则下列说法中正确的是( )
A.物质A、B的转化率之比为1:2
B.起始时刻和达平衡后容器中混合气体密度相等
C.当v正(A)=2v逆(C)时,可断定反应达到平衡状态
D.相同条件下,若起始时放入3molA和3nmolB,则达平衡时生成3amolC
5、选择题 一定条件下,在某容积固定的密闭容器中进行反应:2SO2(g)+O2(g)

?2SO3(g).下列说法中,可以说明反应达到化学平衡状态的是( )
A.SO2、O2、SO3共存
B.SO2、O2、SO3的总质量保持不变
C.SO2、O2、SO3的物质的量浓度不再发生变化
D.以SO2表示的正反应和逆反应速率相等,且等于零