1、选择题 下列反应中生成物总能量高于反应物总能量的是?
A.氢氧化钠溶液与稀硫酸混合
B.异丁醇燃烧
C.氢氧化钡晶体与氯化铵晶体混合搅拌
D.氧化钙溶于水
参考答案:C
本题解析:反应中生成物总能量高于反应物总能量,则该反应为吸热反应。A为中和反应,放热反应;B为燃烧反应,放热反应;C是典型的吸热反应;D氧化钙溶于水,放出大量热量,放热反应。
点评:反应热是历年高考的重点,考生应重点掌握。
本题难度:简单
2、选择题 下列物质加入水中,能发生化学反应且放出热量的是
A.生石灰
B.固体NaOH
C.浓硫酸
D.固体NH4NO3
参考答案:A
本题解析:略
本题难度:简单
3、填空题 用50mL 0.50 mol?L-1盐酸与50mL 0.55 mol?L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图来源:91考试网 91exam.org中尚缺少的一种玻璃用品是??。
(2)烧杯间填满碎纸条的作用是??。
(3)大烧杯上如不盖硬纸板,求得的中和热△H绝对值??。(填偏大、偏小、无影响)
参考答案:(6分)(1)环形玻璃搅拌棒(2)?保温、隔热,减小热量散失对实验造成的影响(3)偏小
本题解析:(1)由于反应中需要搅拌,所以从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒。
(2)该实验中要尽可能的减少热量的损失,所以烧杯间填满碎纸条的作用是保温、隔热,减小热量散失对实验造成的影响。
(3)大烧杯上如不盖硬纸板,则会导致热量的损失,所以求得的中和热△H绝对值偏小。
点评:该题是基础性试题的考查,侧重对学生基础知识的巩固和训练,有利于调动学生的学习兴趣,激发学生的学习积极性。该题主要是常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
本题难度:一般
4、填空题 依据事实,写出下列反应的热化学方程式。
(1)在25℃、101 kPa下,1 g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为?______________________。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为_______________________________________________。
参考答案:(1)CH3OH(l)+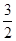 O2(g)===CO2(g)+2H2O(l)?ΔH=-725.76 kJ・mol-1
O2(g)===CO2(g)+2H2O(l)?ΔH=-725.76 kJ・mol-1
(2)N2(g)+2O2(g)===2NO2(g)?ΔH=+67.8 kJ・mol-1
本题解析:(1)燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以1mol甲醇完全燃烧放出的热量是22.68 kJ×32=725.76 kJ,则示甲醇燃烧热的热化学方程式为CH3OH(l)+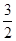 O2(g)===CO2(g)+2H2O(l)?ΔH=-725.76 kJ・mol-1。
O2(g)===CO2(g)+2H2O(l)?ΔH=-725.76 kJ・mol-1。
(2),每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为N2(g)+2O2(g)===2NO2(g)?ΔH=+67.8 kJ・mol-1。
点评:该题是基础性试题的考查,侧重对学生基础知识的训练。该题的关键是明确热化学方程式的含义以及书写注意事项,有利于培养学生规范的答题能力,提高学生的应试能力和学习效率。
本题难度:简单
5、填空题 (2分)如果反应物的总能量小于生成物的总能量,该反应为?反应(填“吸热”或“放热”,下同),盐酸和氢氧化钠的反应属于?反应。
参考答案:吸热、放热
本题解析:略
本题难度:一般