1������� ��8�֣���1�����Ƶ�CuCl2��2H2O�����г�����Fe3+��Fe2+���ʡ����ᴿʱ�����ȼ�����ʵ�����������Fe2+����ΪFe3+�����п�ѡ�õ���������___________��
A.KMnO4?�� B.H2O2?����? C.Cl2ˮ?����? D.HNO3?
(2)��֪��������Ksp��Fe(OH)3��=8.0��10-38,Ksp��Cu(OH)2��=2.2��10-20���S2=0.3��ͨ����Ϊ��������Һ�е�����Ũ��С��1��10-5mol��L-1ʱ����Ϊ������ȫ���Լ���
�ٽ���Һ��pH����PH=__________ʱFe3+ת��ΪFe(OH)3��������ȫ��
����CuSO4��Һ��Ũ��Ϊ2.2mol��L-1����Cu(OH)2��ʼ����ʱ��Һ��pHΪ__________��
(3)������Һ��pH��ѡ�������е�____________��
A.NaOH(aq)? B.NH3��H2O? C.CuO��ĩ? D.Cu(OH)2����Һ? E.Cu2(OH)2CO3(s)
�ο��𰸣�
�����������
�����Ѷȣ�һ��
2��ѡ���� ��t��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp��4��10��10������˵������ȷ����
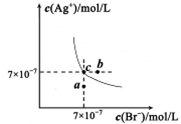
A����t��ʱ��AgBr��KspΪ4.9��10��13
B����AgBr������Һ�м���NaBr���壬��ʹ��Һ��c�㵽b��
C��ͼ��a���Ӧ����AgBr�IJ�������Һ
D����t��ʱ��AgCl(s)��Br��(aq)  AgBr(s)��Cl��(aq)ƽ�ⳣ��K��816
AgBr(s)��Cl��(aq)ƽ�ⳣ��K��816
�ο��𰸣�B
�������������ͼ��c���c(Ag��)��c(Br��)�ɵã����¶���AgBr��KspΪ4.9��10��13��A��ȷ����AgBr������Һ�м���NaBr�����c(Br��)�������ܽ�ƽ�������ƶ���c(Ag��)��С��ƽ������������ϣ�B������a��ʱQc��Ksp����ΪAgBr�IJ�������Һ��C��ȷ��ѡ��D�� ���������ݵ�K��816��D��ȷ��
���������ݵ�K��816��D��ȷ��
�����Ѷȣ�һ��
3��ѡ���� ��ZnSO4��Һ�м���Na2S��Һʱ���õ���ɫ������Ȼ�����ɫ�����еμ�CuSO4��Һ�����ֳ�����Ϊ��ɫ��������˵������ȷ����
A����ɫ����ΪZnS����ɫ����ΪCuS
B����������˵��ZnS��KspС��CuS��Ksp
C�����ø�ԭ����ʵ��һ�ֳ���ת��Ϊ�����ܵij���
D���ù����ƻ���ZnS���ܽ�ƽ��
�ο��𰸣�B
��������������ܽ�ƽ���֪ZnS��Ksp����CuS��Ksp
�����Ѷȣ���
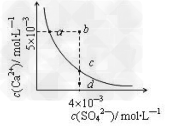
4��ѡ���� �����£�Ksp��CaSO4��=9��10-6��������CaSO4��ˮ�еij����ܽ�ƽ������ͼ������˵����ȷ����
[? ? ]
A��CaSO4��ϡ�����е��ܽ��Ա��ڴ�ˮ�е��ܽ��Դ�
B��a���Ӧ��Ksp����c���Ӧ��Ksp
C��b�㽫�г������ɣ�ƽ�����Һ��c(SO42-)һ������3��10-3 mol/L
D��d����Һͨ���������Ա䵽c��
�ο��𰸣���
���������
�����Ѷȣ���
5��ѡ���� ���жԳ����ܽ�ƽ���������ȷ����
[?]
A����Ӧ��ʼʱ����Һ�и�����Ũ�����
B�������ܽ�ﵽƽ��ʱ�����������ʺ��ܽ���������
C�������ܽ�ﵽƽ��ʱ����Һ�����ʵ�����Ũ����ȣ��ұ��ֲ���
D�������ܽ�ﵽƽ��ʱ������ټ��������Եĸó�������ٽ��ܽ�
�ο��𰸣�B
���������
�����Ѷȣ���