|
高考化学试题《原电池原理》考点特训(2019年冲刺版)(十)
2019-05-30 05:11:07
【 大 中 小】
|
1、填空题 2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)用电子式表示H2O的形成过程 。
(2) H2O以 键结合(填极性键、非极性键、离子键)
(3)在pH=1的溶液中,①NH4+、Al3+、Br-、SO42- ② Na+、Fe2+、Cl-、NO3-
③K+、Ba2+、Cl-、NO3-④K+、Na+、HCO3-、SO42-四组离子中,一定大量共存的是 (填序号)。
(4)在下列反应中,水仅做氧化剂的是 (填字母,下同),水既不做氧化剂又不做还原剂的是 。
A.Cl2+H2O=HCl+HClO
B.2Na2O2+2H2O=4NaOH+O2↑
C.CaH2+2H2O=Ca(OH)2+2H2↑
D.3Fe+4H2O Fe3O4+4H2 Fe3O4+4H2
| (5)已知KH和H2O反应生成H2和KOH,反应中1mol KH (填失去,得到) mol电子
(6)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为 ,电极反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数约为 。
参考答案:(15分) (1) 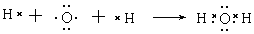 (2分) (2)极性键(1分) (2分) (2)极性键(1分)
(3)①③ (2分)(4)CD(2分) AB(2分) (5)失去(1分) 1(1分)
(6)H2 +2OH - -2e-=2H2O(2分) 200NA (2分)
本题解析:(1)水是以极性键结合的共价化合物,则用电子式表示H2O的形成过程为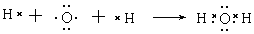 。 。
(3)溶液显酸性,则HCO3-不能大量共存。另外在酸性条件下,NO3-具有强氧化性,能氧化Fe2+,所以一定大量共存的是①③。
(4)在氧化还原反应中,氧化剂得到电子,元素的化合价降低。还原剂失去电子,元素的化合价升高,据此可知A、B中水水既不做氧化剂又不做还原剂的是,CD中水是氧化剂。
(5)KH中H元素的化合价是-1价,反应后变为0价,所以反应中1mol KH失去1mol电子。
(6)原电池中负极失去电子,则氢气在负极通入,电极反应式是H2 +2OH - -2e-=2H2O。生成1mol水转移2mol电子,1.8L水的物质的量是1800g÷18g/mol=100mol,所以反应中转移电子的个数是200NA。
考点:考查电子式、电极反应式、氧化还原反应的有关判断和计算
点评:该题是中等难度的试题,试题基础性强,侧重对学生基础知识的检验。该题主要是以水为载体,重点考查学生对电子式、氧化还原反应以及原电池原理的熟悉了解程度,意在巩固学生的基础,提高学生分析、归纳、总结问题的能力,有利于调动学生的学习兴趣和学习积极性。
本题难度:困难
2、选择题 (2014届上海市十三校高三测试化学试卷)
2013年12月31日夜,上海外滩运用LED产品进行了精彩纷呈的跨年灯光秀。下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是?
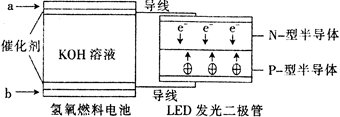
A.a处通入氧气
B.b处为电池正极,发生了还原反应
C.该装置中只涉及两种形式的能量转化
D.P-型半导体连接的是电池负极
参考答案:B
本题解析:
由于电子从在LED发光二极管的N极向P极移动,所以N极与电源的负极连接,P极与电源的正极连接。所以在燃料电池中a处通入的气体为氢气,该处为负极,发生氧化反应;在b处通入的气体为氧气,该处为正极,发生还原反应。在该装置中涉及的能量转化形式有化学能转化为电能,以及电能转化为光能及热能。所以正确选项为B。
本题难度:一般
3、选择题 电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是(? )
A.当电池负极消耗mg气体时,电解池阳极同时有mg气体生成
B.电池负极反应式为:O2 + 2H2O + 4e―= 4OH―
C.电解后c(Na2CO3)不变,且溶液中有晶体析出
D.电池中c(KOH)不变;电解池中溶液pH变大
参考答案:C
本题解析:A.在氢氧燃料电池中通入氢气的电极为负极。当电池负极消耗mg气体时,电子转移的物质的量为mg÷1g/mol=mmol。所以电解饱和碳酸钠溶液,在电解池阳极发生的反应为4OH―-4e―= O2↑+ 2H2O产生氧气的物质的量为m/4mol.因此产生的氧气的质量为m/4mol×32g/mol=8mg。错误。B.在氢氧燃料电池中负极反应式为:H2-2e- + 2OH―= 2H2O 。错误。C.电解饱和碳酸钠溶液,实质就是电解水,所以电解后由于水不断减少,溶液中有晶体析出但是c(Na2CO3)不变。正确。D.电池中n(KOH)不变;由于不断产生水,所以c(KOH)会减小,电解池中溶液pH变小。错误。
本题难度:一般
4、选择题 镍镉(Ni
参考答案:
本题解析:
本题难度:一般
5、填空题 (13分)科学家预言,燃料电池将是21世纪获得电力的重要途径。一种乙醇燃料电池是采用铂或碳化钨作为电极催化剂,在氢氧化钾溶液的电解液中直接加入纯化后的乙醇,同时向一个电极通入空气。回答下列问题:
(1)这种电池放电时发生的化学反应方程式是_____________________________。
(2)此电极的正极发生的电极反应式是__________________________________;
负极发生的电极反应式________________________________。
(3)电解液中的K+离子向______极移动;向外电路释放电子的电极是_____极。
参考答案:(13分)
(1)CH3CH2OH + 3O2 +4KOH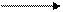 2K2CO3 + 5H2O?(3分) 2K2CO3 + 5H2O?(3分)
(2)O2 +? 2H2O+ 4e- =" 4" OH-?(3分)
CH3CH2OH - 12e- + 16OH- =2CO32- + 11H2O?(3分)
(3)正?(2分) ;?负极?(2分)
本题解析:略
本题难度:一般
|