1、选择题 利用碳酸钠晶体(Na2CO3・10H2O)来配制1.0 mol/L Na2CO3溶液500 mL,假如其他操作均准确无误,下列情况会引起所配溶液浓度偏高的是
[? ]
A.称取碳酸钠晶体53.0 g
B.定容时,俯视观察刻度线
C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗
D.定容后,将容量瓶振荡摇匀,静置后发现液面低于刻度线,于是又加入少量水至刻度线
参考答案:B
本题解析:
本题难度:一般
2、实验题 现用质量分数为98%、密度为1.84 g・cm-3的浓H2SO4来配制500 mL、0.2 mol・L-1的稀H2SO4。可供选择的仪器有:①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有?(填代号)。
(2)经计算,需浓H2SO4的体积为?mL(保留一位小数)。现有①10 mL?②50 mL?③100 mL三种规格的量筒,你选用的量筒是?(填代号)
(3)在配制过程中,其他操作都准确,下列操作中:错误的是?,能引起实验结果偏高的有?(填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓H2SO4
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视标线
参考答案:(1)②⑦⑧ (2分)
(2)5.4mL ?(2分)?;①? (2分)
(3)①?②?③?④?⑥?⑦? (2分)?;①?②?⑦? (2分)
本题解析:
(2)根据稀释定律:C(浓)・V(浓)=C(稀)・V(稀)可得需要浓硫酸5.4mL,量取液体时选择量程相差较小的量筒,所以选择10量筒。
(3)量筒在制造时已经考虑了倒不出来的部分,所以量筒不能再洗涤,否则会导致浓度偏高;容量瓶只能在室温下使用,只有等溶液冷却后才能转移,否则会导致浓度偏高;浓硫酸稀释时,只能往水中缓慢加入浓硫酸并用玻棒不断搅拌;定容时,水超过刻线,只能重新配制;定容摇匀后,有一部分水留在了瓶壁或瓶塞之间,不能加水,否则会导致浓度减小;定容时眼睛要平视凹液面最低处,俯视会导致浓度偏高。所以错误的有①?②?③?④?⑥?⑦。能引起实验结果偏高的有①?②?⑦。
本题难度:一般
3、选择题 NA为阿伏伽德罗常数的值,下列叙述正确的是
A.由D和18O所组成的水11g,所含的中子数为4NA
B.常温常压下,8gO2含有4 NA个电子
C.25℃时,pH=13的1LBa(OH)2溶液中含有OH―的数目为0.2 NA
D.1L1mol/L的NaAlO2水溶液中含有的氧原子数为2NA
参考答案:B
本题解析:A、由D和18O所组成的水11g其物质的量是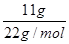 =0.5mol,所含的中子数为(0.5×12)NA=6NA,A不正确;B、常温常压下,8gO2的物质的量是8g÷32g/mol=0.25mol,含有(0.25×16)NA=4NA个电子,B正确;25℃时,pH=13的1LBa(OH)2溶液中氢氧根的浓度是0.1mol/L,则溶液中含有OH―的数目为0.1NA,C不正确;D、溶剂水中含有大量的氧原子,因此1L1mol/L的NaAlO2水溶液中含有的氧原子数大于2NA,D不正确,答案选B。
=0.5mol,所含的中子数为(0.5×12)NA=6NA,A不正确;B、常温常压下,8gO2的物质的量是8g÷32g/mol=0.25mol,含有(0.25×16)NA=4NA个电子,B正确;25℃时,pH=13的1LBa(OH)2溶液中氢氧根的浓度是0.1mol/L,则溶液中含有OH―的数目为0.1NA,C不正确;D、溶剂水中含有大量的氧原子,因此1L1mol/L的NaAlO2水溶液中含有的氧原子数大于2NA,D不正确,答案选B。
本题难度:一般
4、填空题 (9分)填写下列表格
物质
| 分子数
| 质量/g
| 物质的量/mol
| 摩尔质量/g.mol-1
|
H2O
| 3.2×1023
|
|
|
|
N2
|
| 9
|
|
|
HNO3
|
|
| 0.5
|
|
参考答案:
物质
分子数
质量/g
物质的量/mol
摩尔质量/g.mol-1
H2O
3.02×1023
9
0.5
18
N2
3.02×1023
14
0.5
28
HNO3
3.02×1023
31.5
0.5
63
本题解析:考查以物质的量为核心的有关计算。可根据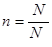 、
、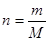 、
、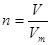 (适用于气体)和
(适用于气体)和 进行有关的计算。
进行有关的计算。
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.5.6g铁粉在2.24L(标准状态)氯气中充分燃烧,失去的电子数为0.3NA
B.常温下,1 molO2和O3的混合气体中所含氧原子数为2.5NA
C.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等
D.13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
参考答案:D
本题解析:A错,铁与氯反应的方程式为:2Fe+3CL2=2FeCL3;5.6g铁粉的物质的量为0.1mol;2.24L(标准状态)氯气物质的量为0.1mol;即氯气的量不足,反应过程中失去的电子数为0.2NA;B错,由于不知道O2和O3的各自的物质的量,本题无解;C错,未指明标准状况;D正确,13.0 g锌的物质的量为0.2 mol;锌与浓硫酸反应或稀硫酸反应均为1 mol锌生成1 mol气体;
本题难度:一般