1��ѡ���� ���и�����������Һ���ܴ����������
A��Cu2+��C1����Na+
B��H+��Cl����CO32��
C��Ba2+��Na+��SO42��
D��H+��K+��OH��
�ο��𰸣�A
���������B�H+����CO32����Ӧ���ɶ�����̼��ˮ�����ܹ��棬�ʴ���C�Ba2+��SO42����Ӧ���ɳ��������ܹ��棬�ʴ���D�H+����OH����Ӧ����ˮ�����ܹ��棬�ʴ�����ѡA��
���������⿼��������ӹ����֪ʶ����Ŀ�ѶȲ����ֽⷴӦ��ʵ�����Ӽ�ķ�Ӧ�����Ӽ䲻���γ�ˮ���������������ӿ��Թ��档
�����Ѷȣ���
2��ѡ���� ��������ǻ�ѧѧϰ�е�һ����Ҫ�������������ƽ�����ȷ���ǣ�������
| ��ȶ��� | ����
A
Cl2+H2O=HCl+HClO
F2+H2O=HF+HFO
B
MgCl2Mg+Cl2��
2AlCl32Al+3Cl2��
C
CH4+Cl2CH3Cl+HCl
CH2=CHCH3+Cl2CH2=CHCH2Cl+HCl
D
Ca��ClO��2+CO2+H2O=CaCO3��+2HClO
Ca��ClO��2+SO2+H2O=CaSO3��+2HClO
|
A��A
B��B
C��C
D��D
�ο��𰸣�A��F2����ǿ�����ԣ���ˮ��Ӧ����������HF����Ӧ�ķ���ʽΪ2F2+2H2O=4HF+O2����A����
B��AlԪ�صĽ����Խ�����AlCl3Ϊ���ۻ��������״̬�²����磬Ӧ�õ���������ķ���ұ������������B����
C�����������ڹ��������·���ȡ����Ӧ����ϩ��������ˮ��������Ȼ�̼��Һ�����ӳɷ�Ӧ����C��ȷ��
D��HClO����ǿ�����ԣ���SO2���л�ԭ�ԣ����߷���������ԭ��Ӧ����D����
��ѡC��
���������
�����Ѷȣ���
3��ѡ���� ij��Һ���������Ӽ���Ũ�����±�����Mn+��aֵ����Ϊ
��������
| NO3-
| SO42-
| H+
| Na+
| Mn+
|
Ũ�ȣ�mol/L��
| 3
| 1
| 2
| 1
| A
|
A��Mg2+��1? B��Ba2+��0.5? C��Al3+��1.5? D��Fe2+�� 2
�ο��𰸣�A
������������ݵ���غ��֪���D3�D2��2��1��nA="0," nA=2,ѡ��A��ȷ������Ǵ���ģ���ѡA��
�����Ѷȣ�һ��
4������� (7��)��1����ͭ��ϡ����Ļ�����м���˫��ˮ��Һ�����Թ۲쵽��ʵ�������ǣ���Һ��������������ɫ���壬��д���漰��һ��������л�ѧ��Ӧ����ʽ��
����������������������������������������������������������������������?��
��2������������ԭ��Ӧ�����ӷ���ʽ���£�
�� R3����Cl2��6OH����RO3����2Cl����3H2O
�� 5RO3����2Mn2����14H����5R3����2MnO4����7H2O
�ɴ�������������ܡ����ܡ����ó�Cl2�������Ա�MnO4��ǿ�Ľ��ۣ���������������������������������������������������������������������������������
�ο��𰸣�

�����������1����������Һ�У�˫��ˮ�ܽ�ͭ�������䷴Ӧ����ʽΪ��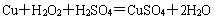 ����Ӧ�����ɵ�ͭ���ӿ���Ϊ˫��ˮ�ֽ�ʱ�Ĵ������ã����ԣ���������ɫ����ķ�Ӧ����ʽΪ��
����Ӧ�����ɵ�ͭ���ӿ���Ϊ˫��ˮ�ֽ�ʱ�Ĵ������ã����ԣ���������ɫ����ķ�Ӧ����ʽΪ�� ��
��
��2������������Ӧ���ڲ���ͬһ�����½��еķ�Ӧ�����ԣ����ܵó�Cl2�������Ա�MnO4��ǿ�Ľ��ۣ�
�����Ѷȣ���
5��ѡ���� �������������Һ����μ���һ����NaOH��Һ������Ϊʵ������з�����Ӧ�����ӷ���ʽ�����д������
A.NH4++2HSO3-+3OH-��NH3?H2O+2SO32-+2H2O
B.NH4++HSO3-+2OH-��NH3?H2O+SO32-+H2O
C.2NH4++HSO3-+3OH-��2NH3?H2O+SO32-+H2O
D.2NH4++5HSO3-+7OH-��2NH3?H2O+5SO32-+5H2O
�ο��𰸣�C
����������������������������Һ����μ���һ����NaOH��Һ�����ȷ�����ӦOH-+HSO3-=SO32-+H2O��HSO3-��Ӧ��ϣ�ʣ���OH-����NH4+������ӦNH4++OH-=NH3?H2O�������������Һ��n��NH4+��=n��HSO3-����������ˮ�⣩�������ӷ���ʽ��HSO3-��ϵ�����ڻ����NH4+��ϵ�������ѡ���жϣ�
����������������Һ����μ���һ����NaOH��Һ�����ȷ�����ӦOH-+HSO3-=SO32-+H2O��HSO3-��Ӧ��ϣ�ʣ���OH-����NH4+������ӦNH4++OH-=NH3?H2O�������������Һ��n��NH4+��=n��HSO3-����������ˮ�⣩�������ӷ���ʽ��HSO3-��ϵ�����ڻ����NH4+��ϵ����
A��NH4++2HSO3-+3OH-=NH3?H2O+2SO32-+2H2O�з�����Ӧ2OH-+2HSO3-=2SO32-+2H2O��NH4++OH-=NH3?H2O������������������������ʵ���֮��Ϊ2��3��笠�����δ��ȫ��Ӧ�����Ϸ�Ӧ����A��ȷ��
B��NH4++HSO3-+2OH-=NH3?H2O+SO32-+H2O�з�����ӦOH-+HSO3-=SO32-+H2O��NH4++OH-=NH3?H2O������������������������ʵ���֮��Ϊ1��2������ǡ����ȫ��Ӧ����B��ȷ��
C��2NH4++HSO3-+3OH-=2NH3?H2O+SO32-+H2O��ʾ���ȷ�����ӦNH4++OH-=NH3?H2O����C����
D��2NH4++5HSO3-+7OH-=2NH3?H2O+5SO32-+5H2O�з�����Ӧ5OH-+5HSO3-=5SO32-+5H2O��2NH4++2OH-=2NH3?H2O������������������������ʵ���֮��Ϊ5��7��笠�����δ��ȫ��Ӧ�����Ϸ�Ӧ����D��ȷ��
��ѡC��
���������⿼�����ӷ���ʽ����д���жϣ��Ѷ��еȣ�ȷ�����ӷ�Ӧ���Ⱥ�˳���ǹؼ���
�����Ѷȣ���