1、选择题 据媒体报道,日本食品巨头明治公司生产的“明治STEP”奶粉中检测出含量超标的放射性元素铯(Cs)。铯较为稳定的核素有 Cs、
Cs、 Cs、
Cs、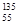 Cs、
Cs、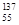 Cs。下列判断不正确的是( )
Cs。下列判断不正确的是( )
A. Cs、
Cs、 Cs、
Cs、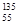 Cs、
Cs、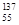 Cs互为同位素
Cs互为同位素
B. Cs、
Cs、 Cs、
Cs、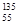 Cs、
Cs、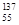 Cs的核外电子排布相同
Cs的核外电子排布相同
C. Cs、
Cs、 Cs、
Cs、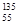 Cs、
Cs、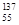 Cs的性质和用途相同
Cs的性质和用途相同
D. Cs、
Cs、 Cs、
Cs、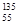 Cs、
Cs、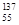 Cs的质量数和中子数均不同
Cs的质量数和中子数均不同
参考答案:C
本题解析:选项A,相同元素的不同核素互为同位素,A正确。选项B,这四种核素是相同的元素,核外电子数相同,B正确。选项C,不同核素的性质有差异,用途也不同,C错。选项D,相同元素的不同核素,其质子数、核外电子数均相同,但中子数、质量数均不同,D正确。
点拨:本题考查同位素、核素及原子结构知识,意在考查考生的知识迁移能力。
本题难度:一般
2、选择题 下图所示是短周期的一部分。已知B原子与C原子核外电子总数之和为A的4倍,则下列推断正确的是?
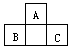
A.A,B,C三者均为非金属元素
B.A,B,C三者核电荷数之和为40
C.A与B,A与C均可形成离子化合物
D.B与C只能形成一种共价化合物
参考答案:A、B
本题解析:短周期:1,2,3周期中含 元素数分别为2,8,8。设B元素的核电荷数为x,则C的核电荷数为(x+2),A的核电荷数为x+1-8=(x-7),4(x-7)=x+x+2,解得x=15。即B为磷(P),A为氧(O),C为氯(Cl)。可见选项A,B正确;C错误,因为P,O,Cl之间不能形成离子化合物;D错误,因Cl与P可形成两种化合物PCl3和PCl5。
本题难度:一般
3、选择题 下列各组物质中,按单质、化合物、混合物顺序排列的是
A.铜、空气、水
B.氧气、干冰、浓硫酸
C.生石灰、熟石灰、烧碱
D.纯碱、水银、胆矾
参考答案:B
本题解析:单质是由同一种元素组成的纯净物,化合物是由不同的元素之间组成的纯净物,混合物是由不同物质的分子组成的物质.
本题难度:简单
4、填空题 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数。R是由A、D两元素形成的离子化合物,其中A+与D2一离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体内晶体类型应属于?(填写“六方”、“面心立方”或“体心立方”)堆积,空间利用率为?。
(2)C3-的电子排布式为?,在CB3分子中C元素原子的原子轨道发生的是?杂化,CB3分子的VSEPR模型为?。
(3)C的氢化物在水中的溶解度如何?,为什么具有这样的溶解性?。
(4)D元素与同周期相邻元素的第一电离能由大到小的关系是:?
(用元素符号表示);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:?。
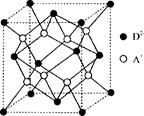
(5)如图所示是R形成的晶体的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是p g・cm-3试计算R晶体中A+和D2-最短的距离?。
(阿伏加德罗常数用NA表示,只写出计算式,不用计算)
参考答案:23. (1)体心立方? 68%?(2)1s2 2s2 2p6? sp3?四面体形?
(3)l:700溶于水或极易溶于水?
氨分子和水分子间可以形成氢键,且氨分子和水分子均为极性分子,相似相溶,氨分子和水分子还可以发生反应,氨气极易溶于水。
(4)C1>P>S?;H2S+Cl2="2HCl+S"
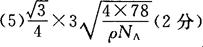
本题解析:B原子得一个电子填入3p轨道后,3p轨道已充满,故B为氯,A+比B-少一个电子层,故A为钠,C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大,氮元素形成的氢化物氨气形成分子间氢键,使溶解度增大,故为N,;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数,故D为硫;(1)钠是体心立方密堆积,空间利用率为 68% ;(2)N3-有8个电子,最外层为全充满,故为1s2 2s2 2p6;NCl3形成三条单键和一对孤对电子,故为sp3杂化,是四面体形;(3)氨气极易溶于水,氨气分子间能形成分子间氢键,且和水均为极性分子,故在水中的溶解度很大;(4)同周期,从左向右整体第一电离能逐渐增大,与硫相邻的为磷和氯,但磷为半充满,稳定,第一电离能大,故C1>P>S;单质间的置换反应可以证明单质氧化性的强弱,故为:H2S+Cl2=2HCl+S;(5)该晶体中钠离子个数为8,硫离子有处于面上的和顶点上的,个数为4,晶胞的体积等于质量除以密度,质量为4个硫化钠的质量,由体积求出立方体的边长,四个硫和一个钠构成正四面体,钠位于正四面体的体心,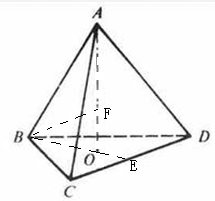 四面体的棱长为晶胞面对角线的一半,由边长求出棱长,根据棱长求出正三角形中BE的长,根据BO和OE的比值为2:1得出BO的长,根据AB和BO求出AO的长,根据三角形中的数量关系求出最短距离。
四面体的棱长为晶胞面对角线的一半,由边长求出棱长,根据棱长求出正三角形中BE的长,根据BO和OE的比值为2:1得出BO的长,根据AB和BO求出AO的长,根据三角形中的数量关系求出最短距离。
本题难度:一般
5、选择题 下列判断错误的是( )
A.熔点:SiO2>NaCl>SiCl4
B.稳定性:AsH3 >PH3> NH3
C.酸性:HClO4>H2SO4>H3PO4
D.碱性:NaOH>Mg(OH)2>Al(OH)3
参考答案:B
本题解析:A选项中SiO2为原子晶体NaCl为离子晶体? SiCl4为分子晶体,而原子晶体的熔点大于离子晶体,离子晶体大于分子晶体,故A选项是正确的。B选项,稳定性的比较,我们可以从比较原子半径大小方面进行比较,原子半径越小,稳定性越强,氮在第二周期,P在第三周期,砷在第四周期,故氮的半径最小,接着到磷,砷最大,故它们的稳定性跟B选项列出来的相反了,所以B选项是错误的。而C、D选项,半径越小酸性越强,半径越大碱性越强,故C、D选项是正确的。
本题难度:一般