1、填空题 A、B、C是在中学化学中常见的3种化合物,它们各由两种元素组成,甲、乙是两种单质,这些化合物和单质之间存在如下的关系:
单质甲? ?化合物A
?化合物A
 ?化合物B?
?化合物B? 化合物B
化合物B
化合物A和化合物C?单质乙和化合物C
据此判断:
(1)在A、B、C这3种化合物中,必定含有乙元素的是??(用A、B、C字母填写)
(2)单质乙必定是??(填“金属”或“非金属”),其理由是??。
(3)单质乙的分子式可能是??,则化合物B的分子式是??
参考答案:(1)A、B
(2)非金属,因为A+B→乙+ C,且乙为单质,可知乙元素在A、B中分别呈正、负价,所以乙是非金属。
(3)S、H2S(或N2、NH3)
本题解析:本题初看起来,题设条件及框图并未给出明的线索,关键在于恰当动用逻辑推理。对于设问(1)化合物A是由甲、乙两种单质化合而成,则化合物A中一定含乙元素;再看左边纵行,单质甲与化合物B反应可生成A(舍乙元素)和C两种化合物,单质甲只含甲元素,则A中的乙元素只能来自化合物B,至于化合物C由题设条件无法判断。因此必定含乙元素的应该是A、B两种化合物。
至于设问(2),则需由框图的右侧纵行推理由化合物A与B(都舍乙元素)反应生成单质乙和化合物C,在单质乙中乙元素的化合价为零价,因此在A、B两种化合物中的乙元素必定分别是正、负两种化合价,因此乙元素必定是非金属元素。这是本题的关键性突破,也是难点。
最后看设问(3),在中学涉及的主要非金属氢、氧、碳、氮、硫、磷、氯中,在其二元化合物中分别呈正、负两种价态以硫、氮为常见。
本题考查了对图表的观察能力以及分析、推理、正向、逆向思维、抽象思维等多种思维能力,也考查了非金属元素的单质及化合物性质的综合认识水平,将化合价的基本概念与具体反应判断相结合,从而从高层次上考查了将化学知识按内在的联系抽象归纳,逻辑地统摄成规律的思维能力。
本题难度:简单
2、选择题 已知次氯酸和次氟酸的分子结构相似,分子中所有原子都形成了稳定结构。下列说法不正确的是
A.次氯酸的结构式为H―O―Cl
B.严格说来,次氯酸的分子应写为HOCl
C.次氟酸应具有很强的氧化性
D.次氟酸中氧元素的化合价为+1价
参考答案:D
本题解析:依据题意分子中所有原子都形成了稳定结构,不难写出其结构式,分别为H―O―Cl和H―O―F。在次氟酸分子中H―O键共用电子对偏向O原子,使O显-1价,O―F键共用电子对偏向F原子,使O显+1价,综上所述,O显0价,次氟酸应具有强化性。
本题难度:一般
3、实验题 饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一。2005年的《化学教育》报道了如下实验研究:
一、定性研究:
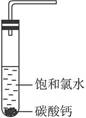
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请完成下列问题:
(1)反应后所得的溶液漂白性增强的原因是____________________________________。
(2)依据上述实验可推知,②的滤液中的溶质除CaCl2、HCIO外,还含有_________。
二、定量研究:
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150 mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加。
请完成下列问题:
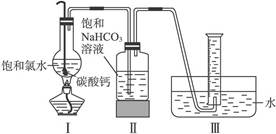
(3)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是____________________________________________________。
(4)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少A g,总共收集到标准状况下的CO2气体B L,发现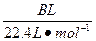 明显小于
明显小于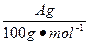 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________________________________________。
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________________________________________。
(5)实验后发现,装置Ⅱ中的液体增多了,其原因是____________________________________。
参考答案:(1)CaCO3消耗了氯水中的HCl,使Cl2+H2O HCl+HClO平衡向右移动,HClO浓度增大
HCl+HClO平衡向右移动,HClO浓度增大
(2)Ca(HCO3)2
(3)在导管末端再连接长导管,使导管的出口接近量筒底部
(4)碳酸钙与CO2反应生成的Ca(HCO3)2使生成CO2的物质的量小于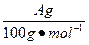
(5)从圆底烧瓶蒸出的水蒸气在广口瓶中冷凝、聚集
本题解析:本题是探索性的实验,研究定性和定量的问题和平衡移动的知识及观察能力、误差分析能力。
由于CaCO3消耗了氯水中的HCl,使Cl2+H2O HCl+HClO平衡向右移动,HClO浓度增大。过量的碳酸钙与释放出的CO2在水中反应生成Ca(HCO3)2。发现
HCl+HClO平衡向右移动,HClO浓度增大。过量的碳酸钙与释放出的CO2在水中反应生成Ca(HCO3)2。发现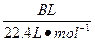 明显小于
明显小于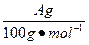 ,原因是CO2并没有完全释放出去。由Ⅰ到Ⅱ会有水蒸发出去,那么在Ⅱ中冷却,所以Ⅱ中的液体增多了。
,原因是CO2并没有完全释放出去。由Ⅰ到Ⅱ会有水蒸发出去,那么在Ⅱ中冷却,所以Ⅱ中的液体增多了。
本题难度:简单
4、选择题 关于盐酸、硫酸、硝酸叙述错误的是
A.三者都是强酸,其稀溶液中只有稀硝酸与铜在常温反应
B.浓盐 酸制氯气,浓硫酸使纸张变黑,浓硝酸常温与铜反应,体现了三
酸制氯气,浓硫酸使纸张变黑,浓硝酸常温与铜反应,体现了三 者的强氧化性
者的强氧化性
C.将强氧化性的浓硫酸与浓硝酸按比例混合可以得到氧化性更强的王水
D.铝、铁在冷的浓硫酸或浓硝酸的钝化属于化学反应
参考答案:BC
本题解析:略
本题难度:一般
5、填空题 (6分)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
?。
(2)漂白粉的有效成分是(填化学式)?。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为?。
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号)?。
参考答案:(1)2Cl2+2Ca(OH)2 = CaCl?2+Ca(ClO)2+2H2O
(2)Ca(ClO)2
(3)Ca(ClO)2 + CO2 + H2O ="=" CaCO3↓+ 2 HClO
(4)(1)
本题解析:略
本题难度:简单