1、选择题 已知Ag2SO4的Kw为2.0×10-3,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO42-浓度随时间变化关系如图〔饱和Ag2SO4溶液中c(Ag+)=0.034 mol・L-1〕。若t1时刻在上述体系中加入100 mL0.020 mol・L-1 Na2SO4溶液,下列示意图中,能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是
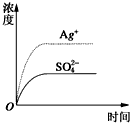
[? ]
A.
B.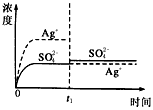
C.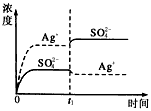
D.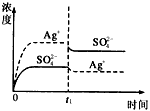
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列说法不正确的是
[? ]
A.向纯水中加入盐酸使水的电离平衡逆向移动,水的离子积减小?
B.反应NH3(g)+HCl(g)==NH4Cl(s)?△H<0,低于一定温度自发,高于一定温度非自发
C.铅蓄电池在放电过程中,负极质量减少,正极质量增加
D.用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3?
参考答案:AC
本题解析:
本题难度:一般
3、选择题 将足量的BaCO3粉末分别加入下列溶液中,充分溶解至溶液饱和.各溶液中Ba2+的浓度最小的为( )
A.10?mL?0.2?mol/LNa2CO3溶液
B.40?mL水
C.50?mL?0.01?mol/L?氯化钡溶液
D.100?mL?0.01?mol/L盐酸
参考答案:A.将足量BaCO3粉末加入10mL0.2mol/LNa2CO3溶液中,由于碳酸根离子的浓度较大,抑制碳酸钡的溶解,则Ba2+的浓度很小;
B.BaCO3粉末加入40mL水中,充分溶解至溶液饱和存在BaCO3(s)?Ba2+(aq )+CO32-(aq),则溶液中存在一定浓度的Ba2+,但浓度较小;
C.将足量BaCO3粉末加入50mL0.01mol/L氯化钡溶液中,氯化钡电离产生0.01mol/LBa2+,则Ba2+的浓度较大;
D.将足量BaCO3粉末加入100mL0.01mol/L盐酸中,碳酸钡与盐酸反应生成0.005mol/LBa2+,则Ba2+的浓度较大;
显然A中Ba2+的浓度最小,
故选A.
本题解析:
本题难度:一般
4、选择题 对于难溶盐MX,其饱和溶液中M+和X-浓度之间的关系为Ksp=c(M+)?c(X-),现将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的顺序是(?)
①20mL0.01mol?L-1?KCl溶液;②30mL0.02mol?L-1CaCl2溶液;③40mL0.03mol?L-1HCl溶液;④10mL蒸馏水;⑤50mL0.05mol?L-1AgNO3溶液
A.①>②>③>④>⑤
B.④>①>③>②>⑤
C.⑤>④>②>①>③
D.④>③>⑤>②>①
参考答案:B
本题解析:根据氯化银的溶解平衡可知,溶液中氯离子浓度或银离子浓度越大,氯化银的溶解度就越小。所以根据溶液中氯离子或银离子浓度大小可知,选项B正确,答案选B。
本题难度:一般
5、填空题 已知二元酸H2A在水中存在以下电离:H2A===H++HA-, HA-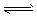 H++A2-,试回答下列问题:
H++A2-,试回答下列问题:
(1)NaHA溶液呈________性,理由是___________。
(2)某温度下,向10 mL 0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至中性,此时溶液中以下关系一定正确的是________(填写字母)。
A.c(Na+)+c(K+)=c(HA-)+c(A2-)
B.水的离子积KW=c2(OH-)
C.V=10
D.c(K+)<c(Na+)
(3)已知难溶物CaA在水中存在溶解平衡;CaA(s) Ca2++A2-;ΔH>0。
Ca2++A2-;ΔH>0。
①温度升高时,Ksp________(填“增大”、“减小”或“不变”,下同)。
②向浊液中通入HCl气体,c(Ca2+)________,原因是_____________。
(4)在粗制CuSO4・5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3。甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol・L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol・L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为_______,通过计算确定上述方案______(填“可行”或“不可行”)。
参考答案:(1)酸 ; HA-只电离不水解
(2)BD
(3)①增大; ②增大; H+与A2-结合为HA-,使平衡右移,c(Ca2+)增大
(4)4 ;?3.3; 可行
本题解析:
本题难度:一般