1、填空题 根据下图所示实验回答下列问题:

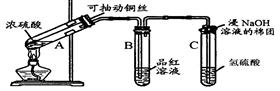
 (1)试管C口部的棉团上发生反应的离子方程式是?。
(1)试管C口部的棉团上发生反应的离子方程式是?。
 (2)试管B中的实验现象是?,若将该试管中反应后的溶液加热,可以观察到?。试管C中溶液变浑浊,则证明SO2具有?性。
(2)试管B中的实验现象是?,若将该试管中反应后的溶液加热,可以观察到?。试管C中溶液变浑浊,则证明SO2具有?性。
 (3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是?,如果浸NaHCO3溶液,则发生反应的化学方程式是?。
(3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是?,如果浸NaHCO3溶液,则发生反应的化学方程式是?。
2、选择题 下列关于浓HNO3和浓H2SO4的叙述,正确的是
A.都不易分解
B.常温下都能与铜较快反应
C.露置在空气中,容器内溶液的质量都减小
D.露置在空气中,容器内溶液的浓度都减小
3、选择题 标准状况下H2S和O2混合气体100mL,经点燃后反应至完全,所得气体经干燥后,恢复到原来状况时体积为10mL,该10mL气体可能是?(?)

A.H2S、SO2
B.O2
C.H2S
D.SO3
4、选择题 下列不能说明氯的非金属性比硫强的事实是?
[?]
①HCl比H2S稳定?②HClO氧化性比H2SO4强?③HClO4酸性比H2SO4强? ④Cl2能与H2S反应生成S?⑤Cl原子最外层有7个电子,S原子最外层有6个电子 ?⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS?⑦HCl酸性比H2S强
A.②⑤⑦?
B.①②⑦?
C.②④?
D.①③⑤
5、选择题 有下列两种转化途径,某些反应条件和产物已省略,下列有关说法不正确的是
途径① S H2SO4
H2SO4
途径② S SO2
SO2 SO3
SO3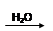 H2SO4
H2SO4
A.途径①反应中体现了浓HNO3的强氧化性和酸性
B.途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本
C.由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e-
D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高