1、简答题 A、B、C、D、E五种化合物均含有某种常见短周期元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)
(1)写出化学式:A______,B______,C______,D______,E______.
(2)写出下列反应的离子方程式:A→B:______;A→D______.
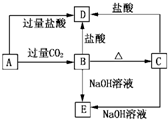
参考答案:B、C都既能与盐酸反应又能与NaOH溶液反应,应为两性化合物,因B加热分解可生成C,则可知B为Al(OH)3,C为A12O3,则D为AlCl3,E为NaAlO2,若取A溶液灼烧,焰色反应为紫色(透过蓝色钴玻璃片),说明A中含有K元素,A能与二氧化碳反应生成Al(OH)3,则A应为KAlO2,
(1)通过以上分析知,A、B、C、D、E分别是KAlO2、Al(OH)3、A12O3、AlCl3、NaAlO2,
故答案为:KAlO2;Al(OH)3;A12O3;AlCl3;NaAlO2;
(2)A→B的反应为AlO2-和Al(OH)3的转化,反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
A→D的反应为AlO2-和Al3+的转化,反应的离子方程式为AlO2-+4H+=Al3++2H2O,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;AlO2-+4H+=Al3++2H2O.
本题解析:
本题难度:简单
2、填空题 已知X为一种盐,A、C、D、F为无色气体,B常温常压下为无色无味的液体,I和Y为中学化学常见的单质,其中Y为气体,I为紫红色固体,E为黑色固体氧化物,L为蓝色沉淀。其中有些反应的条件及部分生成物被略去。
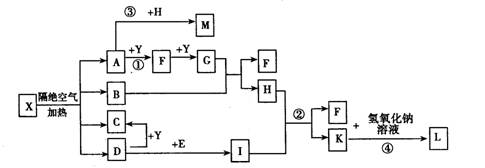
回答下列问题:
(1)写出C的电子式?,L的化学式?。
(2)写出反应①的化学反应方程式_?___;反应①一④中属于氧化还原反应的是?。
(3)写出反应②的离子反应方程式__?__。
(4)M的水溶液呈酸性,其原因为(用离子方程式表示)__?__。
(5)利用电解可提纯I物质,在该电解反应中电解质溶液是__?__;写出阴极的电极反应式___?_。
(6)已知1 mol X在隔绝空气条件下分解产生的各产物的物质的量之比为A:B:C:D=2:1:1:1请推测A的化学式为___?_。
参考答案: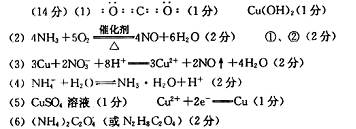
本题解析:略
本题难度:一般
3、推断题 现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
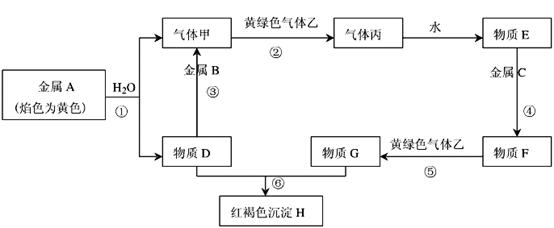
请回答下列问题:
(1)写出下列物质的化学式:B_________、丙_________、乙_________。
(2)写出下列反应的离子方程式:
反应①_____________________________________________;
反应⑤_____________________________________________;
反应⑥_____________________________________________。
参考答案:(1)Al、HCl、Cl2
(2)2Na+2H2O=2Na++2OH-+H2↑;Cl2+2Fe2+=2Fe3++2Cl- ;Fe3++3OH-=Fe(OH)3↓
本题解析:金属A的焰色反应是黄色,说明A是Na。钠和水反应生成氢氧化钠和氢气,则甲是氢气,D是氢氧化钠。乙是黄绿色气体,则乙是氯气。氯气和氢气化合生成氯化氢,则丙是氯化氢。氯化氢溶于水生成盐酸,则E是盐酸。红褐色沉淀H应该是氢氧化铁,氢氧化钠和G反应生成氢氧化铁,所以G是氯化铁。F和氯气反应生成氯化铁,则F是氯化亚铁,因此金属C是铁。
点评:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合。它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法。解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。
本题难度:一般
4、填空题 (10分)已知A为酸式盐,B为某二价主族金属元素的化合物,常温常压下C、D、F、G、I均呈气态。等物质的量A、B与少量的水充分混合能恰好完全反应。图中反应条件(除高温外)均已略去。请回答下列问题:
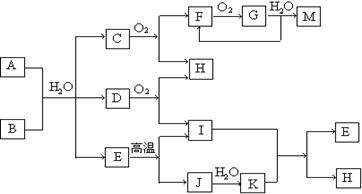
(1)写出B的电子式?,
(2)写出A与B反应的化学方程式?。
(3)如对气体 G进行加压操作,产生的现象是?。
G进行加压操作,产生的现象是?。
(4)写出下列反应的离子方程式:
①在A溶液中加入M?。
②向A溶液中加入过量NaOH 溶液,并加热?。
溶液,并加热?。
参考答案:A:NH4HCO3? B: CaC2? C:NH3? D:C2H2
E:CaCO3 F:NO G:NO2? H:H2O? I:CO2? J:CaO? K:Ca(OH)2? M:HNO3
本题解析:略
本题难度:一般
5、填空题 A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件未标出),其中反应①是置换反应。
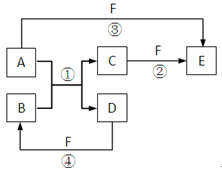
(1)若A、D、F都是非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是:?。
(2)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是:?。
(3)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,③和④两个反应中都有红棕色气体生成,B的结构式是:?;反应④的化学方程式是:?。
参考答案:(1)2C+SiO2 Si+2CO?(2)2Fe2++Cl2=2Fe3++2Cl-
Si+2CO?(2)2Fe2++Cl2=2Fe3++2Cl-
(3)O=C=O? C+4HNO3(浓)=4NO2↑+CO2↑+2H2O
本题解析:(1)若A、D、F都是非金属单质,反应①是置换反应,A、D同主族,根据框图可知,A与F生成E,C与F也能生成E,因此只能是SiO2与C反应,则A是C、B是SiO2、C是CO、D是Si,E是CO2、F是O2。
(2)若A是常见的金属单质,反应①是置换反应,D、F是气态单质,根据框图可知,A与F生成E,C与F也能生成E,因此A只能为Fe,D为H2,F为Cl2,B为HCl,C为FeCl2,E为FeCl3。
(3)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,反应①是置换反应,根据框图可知,A为Mg,D为C,B为CO2,C为MgO,又知③和④两个反应中都有红棕色气体生成,F为HNO3。
点评:本题综合性强,难度较大,一个框图适用三种情况,这要求学生对物质之间的反应必须熟练,尤其本题还涉及到了置换反应,在高中所学的置换反应是有限的,可以好好总结一下,能够提高做这类习题的效率。
本题难度:一般