1���ƶ��� ��֪A��B��E�dz����ķǽ������ʣ�C�ǵ����������Ҫ�ɷ�֮һ��Y�������г����Ľ������ʡ�D��K����Ҫ����������Ʒ��X��������Ԫ�أ�����ҡ��ʽ�ķ��ӽṹ�������ģ����ͼ��ʾ��HΪ��ɫ����������ת����ϵ�в��ַ�Ӧ�����Ͳ�����ȥ��

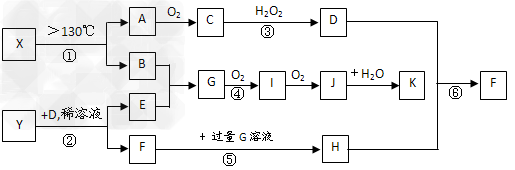
�Իش���������
��1��X�Ļ�ѧʽΪ______________��G�ĵ���ʽ______________��
��2����Ӧ�ܵĻ�ѧ����ʽ_______________________����Ӧ�۵����ӷ���ʽ____________________________��?
��3����ˮϡ��0.1?mol/LG��Һʱ����Һ������ˮ�������Ӷ���С����_______(��д���)? ��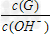 ?��
?��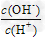 ?��?c��H+����c��OH-���ij˻�?��?OH�������ʵ���
?��?c��H+����c��OH-���ij˻�?��?OH�������ʵ���
��4�������£���0.01mol/L?G��Һ�еμ�0.01mol/L?D��Һ�����ԣ��õ�����Һ���������ӵ����ʵ���Ũ���ɴ�С��˳��Ϊ_______________��
��5����~��Ӧ������������ԭ��Ӧ���ǣ����ţ�___________��
��6������ʵ���е�����ʵ������ȷ��Y�Ǻ��ֽ�������ʵ������Ϊ____________��
�ο��𰸣���1��S4N4?��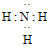 ?
?
��2��4NH3��5O2��4NO��6H2O��SO2��H2O2��2H+��SO42��?
��3���٢�
��4��c(NH4��)>c(SO42��)>c(OH��)=c(H��)?
��5���٢ڢۢ�?
��6����ɫ����H�����ڿ����У�����ɰ�ɫ��ɺ��ɫ����Ϊ������֮Ϊ��
���������
�����Ѷȣ�һ��
2������� ��7�֣���A��B��C��D���ֵ��ʡ���һ�������£�B���Ժ�A��C��D�������ɻ�����ס��ҡ�����C��D�������ɻ����ﶡ����֪�ס��ҡ���ÿ�������ж�����10�����ӣ����Ҽס��ҡ������������¹�ϵ��
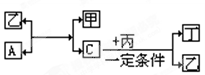
�ش�
��1������B�Ļ�ѧʽ��
��2������A�뻯�����ҷ�Ӧ�Ļ�ѧ����ʽ��
��3�����ݻ������������D Ԫ�ػ��ϼ��жϱ������Ƿ���һ�����������ɵ���D�������ж����ɡ�
Ԫ�ػ��ϼ��жϱ������Ƿ���һ�����������ɵ���D�������ж����ɡ�
�ο��𰸣�

�����������
�����Ѷȣ���
3������� ����Ϊ��ѧ�������ʣ�ת����ϵ���£�C��B��Һ��Ӧ��������F��D����F��ȼ�գ�ͼ�в��ֲ�����ȥ��
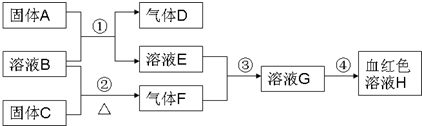
��1��д������C��ѧʽ______��
��2��ʵ�����â���ȡD��B��ҺӦΪ______��Һ����Ũ����ϡ���������â���ȡF��B��ҺӦΪ______��Һ����Ũ����ϡ������д���ڷ�Ӧ����ʽ______��
��3����μ���E�е�������______��
��4��ʵ��������G��Һ������Ϊ______��
��5�����ۿ�ʵ��E��G�⣬������������ʵ��E��G����ѧ����ʽ______��
��6��4gD�ڿ�������ȫȼ������Һ������ʱ���ų�����ΪQkJ��д���÷�Ӧ���Ȼ�ѧ����ʽ______��
�ο��𰸣���ҺHΪѪ��ɫ��ΪFe��SCN��3����ת����ϵ��֪����ҺG����Fe3+���ɷ�Ӧ�ۿ�֪����ҺE����FeԪ�أ��ɷ�Ӧ�ٹ���A+��ҺB����ҺE+����D������Fe����ķ�Ӧ��AΪFe��BΪ�ᣬDΪH2��EΪ�����Σ��ɷ�Ӧ�ۿ�֪����F����ǿ�����ԣ���Ϸ�Ӧ����ҺB+����C��
���������
�����Ѷȣ�һ��
4������� a��b��c��d��e��f��gΪ������1��18��Ԫ�ع��ɵ��������Ƕ���10�����ӣ���ṹ�ص����±���
| ������ | a | b | c | d | e | f | g
ԭ�Ӻ���
����
����
���
����
˫��
���
���
��������
1+
2-
0
3+
1-
0
1+
|
����b�����Ӱ뾶����d�����Ӱ뾶��c����ԭ�ӷ��ӣ�e��g���ȿ��γ�c��f���ַ��ӣ���д����
��1��c���ӵĽṹʽΪ______��
��2��a��e����������ɻ�����ĵ���ʽΪ______��
��3��a�ĵ�����f��Ӧ�Ļ�ѧ����ʽ______��
��4��d������a��e����������ɻ�������Һ��Ӧ�����ӷ���ʽ______��
�ο��𰸣�aΪNa+��bΪO2-��c����ԭ�ӷ��ӣ�ӦΪNH3��dΪAl3+��eΪOH-��e��g���ȿ��γ�c��f���ַ��ӣ���gΪNH4+��fΪH2O��
��1��c��ԭ�ӷ��ӣ�ӦΪNH3���ṹʽΪ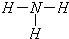 ���ʴ�Ϊ��
���ʴ�Ϊ��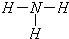 ��
��
��2��aΪNa+��eΪOH-���γɵĻ�����ΪNaOH��Ϊ���ӻ��������ʽΪ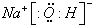 ���ʴ�Ϊ��
���ʴ�Ϊ��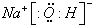 ��
��
��3������ˮ��Ӧ�����������ƺ���������Ӧ�Ļ�ѧ����ʽΪ2Na+2H2O�T2NaOH+H2�����ʴ�Ϊ��2Na+2H2O�T2NaOH+H2����
��4����������������Һ��Ӧ����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O�T2AlO2-+3H2�����ʴ�Ϊ��2Al+2OH-+2H2O�T2AlO2-+3H2����
���������
�����Ѷȣ�һ��
5������� ��14�֣�A��B��C��D��E����ѧ��ѧ������5�ֻ��������A��B�����������X��Y�������г����Ľ�����������ʼ��ת�� ��ϵ����ͼ��ʾ�����ַ�Ӧ�����������ȥ����
��ϵ����ͼ��ʾ�����ַ�Ӧ�����������ȥ����

��1�����Լ�l���Լ�2������ͬ�����ʣ���X���Լ�l��Ӧ�����ӷ���ʽ��? ?��
?��
��2�����Լ�1���Լ�2��ͬ����E��Һ�������ɲ����պ�ɵõ�A����A�Ļ�ѧʽ��?��
�ټ�������D����Һ�н����� �ӵ�ʵ�������?��
�ӵ�ʵ�������?��
�ڽ�����C����ˮ������Һ��?������ԡ��������ԡ����ԡ�����ԭ�������ӷ���ʽ�ɱ�ʾΪ?��
��3����E��Һ���������������ɺ�ɵõ�����Һ�����ʣ���ҵ����E��ϡ�����NaNO2Ϊԭ�����Ʊ���Ч��ˮ��Y��OH��SO4����Ӧ����N0���ɣ��÷�Ӧ�Ļ�ѧ����ʽ��?��
�ο��𰸣���14�֣�
��1��2Al + 2H2O + 2OH��=2AlO2��+ 3H2����2�֣�
��2��Fe2O3��2�֣�
��ȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ���ɫ����֤��ԭ��Һ�к���Fe3+��3�֣������������𰸣�
�����ԣ�2�֣���Al3+ + 3H2O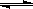 ?Al(OH)3 + 3H+��2�֣�
?Al(OH)3 + 3H+��2�֣�
��3��2FeSO4 + 2NaNO2 + H2SO4��2Fe(OH)SO4 + Na2SO4 + 2NO����3�֣�NaHSO4Ҳ�ɣ�
�����������
�����Ѷȣ���