1������� ������ѧ��ѧ�г������ʵ�ת����ϵͼ�У���Ӧ���������ַ�Ӧ��Ͳ���δȫ��ע������֪A��DΪ�������ʣ�����Ϊ�����
���ƶϣ�
��1��д�����ʵĻ�ѧʽ��A��______��C��______��I��______��
��2��д�����з�Ӧ�ķ���ʽ��
C��F�����ӷ���ʽ______��
H��I�Ļ�ѧ����ʽ______��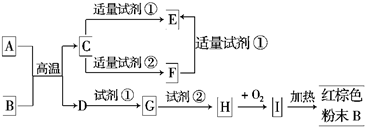
�ο��𰸣���BΪ����ɫ��ĩ��֪��BΪFe2O3�����ת����ϵͼ��֪��IΪFe��OH��3��HΪFe��OH��2��GΪFeCl2��DΪFe��A+B��D+CΪ���ȷ�Ӧ����AΪAl��CΪAl2O3��EΪAlCl3��FΪƫ�����Σ������Լ���Ϊ���ᣬ�Լ���Ϊǿ���NaOH��KOH�ȣ���
��1��������������֪��AΪAl��CΪAl2O3��IΪFe��OH��3���ʴ�Ϊ��Al��Al2O3��Fe��OH��3������
��2��C��F�����ӷ���ʽΪAl2O3+2OH-�T2AlO2-+H2O��H��I�Ļ�ѧ����ʽΪ4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
�ʴ�Ϊ��Al2O3+2OH-�T2AlO2-+H2O��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
���������
�����Ѷȣ�һ��
2������� A��B��C��D��E�������ʾ�����ͬһ��Ԫ�أ�����֮��������ת����ϵ��
��1����AΪ���ʣ�B��C���������࣬B��ˮ��Һ�����ԣ�C��ˮ��Һ�ʼ��ԣ�D��һ�ְ�ɫ������д�����й��̵����ӷ���ʽ��
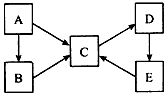
��B��ˮ��Һ������____________�� ��C��D_______________�� ?��E��C________________��
��2����A��E��Ϊ�����A�ǵ���ɫ���壻B��C����Һ�ڵ����ʵ���Ũ��ʱ��C ��Һ��pH��С�����D��ˮ��Һ������Ҫ�Ĺ�ҵ����֮һ��D��E��CҲ�ǹ�ҵ�Ʊ�C���ձ鷽����?
��A�ĵ���ʽΪ__________��?
�ڵ��D��ˮ��Һʱ����Ӧ�����ӷ���ʽΪ________________��
����������D��Һ��������ʴ�������ĵ缫��ӦΪ________________��?
��3����AΪ���ʣ�C��D����Է����������16��0.1mol/L E��Һ��ֻ��3�����ӣ��ҳ�������Һ�е�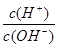 =1012��
=1012��
��B��C�Ļ�ѧ����ʽΪ��?��
��A��C�ķ�Ӧ�У�ÿת��1 mol e-�ͻ�����45 kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ��?��
�ο��𰸣���1����Al3++3H2O  ?Al(OH)3+3H+��?��AlO2-+H++H2O=Al(OH)3��?��Al2O3+2OH-=2AlO2-+H2O
?Al(OH)3+3H+��?��AlO2-+H++H2O=Al(OH)3��?��Al2O3+2OH-=2AlO2-+H2O
��2���� �� ?��2Cl-+2H2O
�� ?��2Cl-+2H2O H2��+Cl2��+2OH-��?��O2+4e-+2H2O=4OH-
H2��+Cl2��+2OH-��?��O2+4e-+2H2O=4OH-
��3����4NH3+5O2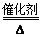 4NO+6H2O?��N2(g)+O2(g)=2NO(g)?��H="+180" kJ/mol
4NO+6H2O?��N2(g)+O2(g)=2NO(g)?��H="+180" kJ/mol
�����������1�������������֪��A��Al ;? B:AlCl3;? C:NaAlO2; D:Al(OH)3;? E:Al2O3.��B��ˮ��Һ����������ΪAlCl3��ǿ�������Σ����������ˮ��������ˮ���������OH-�����յ���Һ�ﵽƽ��ʱ��C(H+)>C(OH-).ˮ������ӷ���ʽΪ��Al3++3H2O  Al(OH)3+3H+ ��C��D AlO2-+H++H2O=Al(OH)3����E��C? Al2O3+2OH-=2AlO2-+H2O
Al(OH)3+3H+ ��C��D AlO2-+H++H2O=Al(OH)3����E��C? Al2O3+2OH-=2AlO2-+H2O
��2�� ��A��E��Ϊ�����A�ǵ���ɫ���壻B��C����Һ�ڵ����ʵ���Ũ��ʱ��C ��Һ��pH��С�����D��ˮ��Һ������Ҫ�Ĺ�ҵ����֮һ��D��E��CҲ�ǹ�ҵ�Ʊ�C���ձ鷽����?������ʷֱ��ǣ�A ��Na2O2; B :NaOH; C :Na2CO3;D : NaCl;E :NaHCO3. ��Na2O2�ĵ���ʽΪ .�ڵ�ⱥ��NaCl��ˮ��Һ�����ӷ���ʽΪ2Cl-+2H2O
.�ڵ�ⱥ��NaCl��ˮ��Һ�����ӷ���ʽΪ2Cl-+2H2O H2��+Cl2��+2OH-������������NaCl��Һ����������������ʴ�������ĵ缫��ӦΪO2+4e-+2H2O=4OH-�������ĵ缫ʽΪFe-2e-=Fe2+.
H2��+Cl2��+2OH-������������NaCl��Һ����������������ʴ�������ĵ缫��ӦΪO2+4e-+2H2O=4OH-�������ĵ缫ʽΪFe-2e-=Fe2+.
��3����AΪ���ʣ�C��D����Է����������16��0.1mol/L E��Һ��ֻ��3�����ӣ��ҳ�������Һ�е�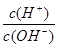 =1012����A��N2��B��NH3��C��NO��D��NO2��E��HNO3����B��C�Ļ�ѧ����ʽΪ��4NH3+5O2
=1012����A��N2��B��NH3��C��NO��D��NO2��E��HNO3����B��C�Ļ�ѧ����ʽΪ��4NH3+5O2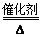 4NO+6H2O��A��C�ķ�Ӧ���Ȼ�ѧ����Ϊ��N2(g)+O2(g)=2NO(g)?��H="+180" kJ/mol��
4NO+6H2O��A��C�ķ�Ӧ���Ȼ�ѧ����Ϊ��N2(g)+O2(g)=2NO(g)?��H="+180" kJ/mol��
�����Ѷȣ�����
3������� ���и����ʵ��ת���У���Ӧ�١����ǹ�ҵ����Ҫ�ķ�Ӧ��A����Է�������Ϊ120��X�������������Ѫ�쵰��϶�ʹ���ж���Y���������ЧӦ��D���γ����꣬E�dz����Ľ�����F���ӵĽṹ��Y���ӵĽṹ���ƣ���F����Է�������Ϊ60��
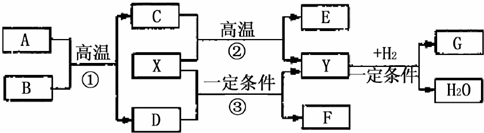
�ش��������⣺
��1��д���������ʵĻ�ѧʽ��A______��E______��
��2����Ӧ�ٵĻ�ѧ����ʽΪ______��
��3����Ӧ�ڵĻ�ѧ����ʽΪ______��
��4��д��F�Ľṹʽ______��
��5��Y��H2��һ�������¿����ɶ������ʣ��ȿɻ�þ���Ч�棬Ҳ�ɼ���Ի�������Ⱦ��
����G��һ��ȼ�ϣ�����Է���������B����Է���������ȣ���G�Ľṹ��ʽΪ______��
����G��Y��H2��1��3�ı�����Ӧ���õ������л����G������______��
�ο��𰸣�Y���������ЧӦ��YΪCO2��D���γ����꣬ΪSO2��X�������������Ѫ�쵰��϶�ʹ���ж������ת���ڿ�֪XΪCO��E�dz����Ľ�����E������Fe��CΪ�����������Ϸ�Ӧ�ټ�A����Է�������Ϊ120��֪����Ӧ��ΪFeS2+O2��Fe2O3+SO2��AΪFeS2��BΪO2��CΪFe2O3������ת����ϵ��
F���ӵĽṹ��Y���ӵĽṹ���ƣ�F����Է�������Ϊ60���ɷ�Ӧ��CO+SO2��CO2+F��FΪO�TC�TS��
��1��������������֪��AΪFeS2��EΪFe��
�ʴ�Ϊ��FeS2��Fe��
��2����Ӧ����FeS2��O2��Ӧ�������������������Ӧ����ʽΪ��4FeS2+11O2?����?.?2Fe2O3+8SO2��
�ʴ�Ϊ��4FeS2+11O2?����?.?2Fe2O3+8SO2��
��3����Ӧ����һ����̼����������Ӧ��������������̼����Ӧ����ʽΪ��Fe2O3+2CO?����?.?2Fe+3CO2��
�ʴ�Ϊ��Fe2O3+2CO?����?.?2Fe+3CO2��
��4��F���ӵĽṹ��Y���ӵĽṹ���ƣ�F����Է�������Ϊ60���ɷ�Ӧ��CO+SO2��CO2+F��FΪO�TC�TS��
�ʴ�Ϊ��O�TC�TS��
��5����ת����ϵCO2+H2��G+H2O��
����G��һ��ȼ�ϣ�����Է���������O2����Է���������ȣ���GΪCH3OH��
�ʴ�Ϊ��CH3OH��
����G��CO2��H2��1��3�ı�����Ӧ���õ������л������Ԫ���غ��֪G��Cԭ����Hԭ����ĿΪ1��2����G����ΪC2H4��
�ʴ�Ϊ��C2H4��
���������
�����Ѷȣ�һ��
4��ѡ���� ����H2SO4��BaCl2��K2CO3��FeSO4����ˮ������Һ������ͼ��ʾ�����ϵ��ͼ��ÿ���������˵����ʿ��Է�����ѧ��Ӧ�������ƶϲ��������ǣ�?��
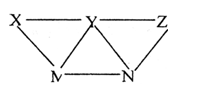
A��Xһ��ΪH2SO4
B��Yһ��ΪK2CO3
C��Z��������ˮ
D��M����ΪFeSO4
�ο��𰸣�A
���������K2CO3���������������ʷ�Ӧ������Y��K2CO3��H2SO4����BaCl2��K2CO3�������ʷ�Ӧ����ˮ����K2CO3��FeSO4�������ʷ�Ӧ������X��Z������H2SO4����ˮ��BaCl2��H2SO4��K2CO3��FeSO4�������ʷ�Ӧ��FeSO4����BaCl2��K2CO3����ˮ�������ʷ�Ӧ������M��N������BaCl2��FeSO4��
�����Ѷȣ�һ��
5���ƶ��� V��W��X��Y��Z�������ڱ���1~ 20�Ų���Ԫ����ɵ�5�ֻ��������V��W��X��Z��Ϊ����Ԫ����ɡ�����5�ֻ������漰������Ԫ�ص�ԭ������֮�͵� ��35������֮��ķ�Ӧ��ϵ����ͼ
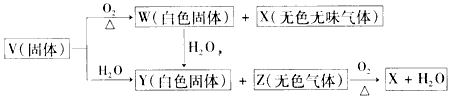
��1��5�ֻ�����ֱ���V_________��W_________��X_________��Y_________��Z_________�����ѧʽ��
��2��������5�ֻ������е�ij2�ֻ����ﷴӦ������һ���»������������5�ֻ������е�����Ԫ�أ����ɸû�����Ļ�ѧ����ʽ��___________________________��
��3��V�ĵ���ʽ��_____________________��
�ο��𰸣���1��CaC2��CaO��CO2��Ca(OH)2��C2H2?
��2��Ca(OH)2+2CO2==Ca(HCO3)2?
��3��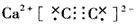
���������
�����Ѷȣ�һ��