1��ѡ���� ���������У����й��ۼ������ӻ�������
[? ]
A��Na2O2
B��MgCl2
C��NH3
D��KCl
�ο��𰸣�A
���������
�����Ѷȣ���
2��ѡ���� ����˵������ȷ���ǣ�?��
A��NO2��SO2��BF3����������ԭ�ӵ��������Ӷ�������8e���ȶ��ṹ
B��P4��CH4����������������Ҽ��Ƕ�Ϊ109o28�@
C��CsCl��������ÿ��Cs+��������������Cl-����8��
D��ԭ�Ӿ�����۷е�һ���Ƚ�������ĸ�
�ο��𰸣�C
������������ۻ�������Ԫ�ػ��ϼ۵ľ���ֵ������������֮������8�����Ԫ��ԭ�ӵ��������Ӿ�������8�����ȶ��ṹ������A��N��S��B�������㣬A����ȷ�����ļ�����60��ģ�B����ȷ��ԭ�Ӿ�����۷е㲻һ���Ƚ�������ĸߣ������ٵ��۷е�ͺܸߣ�D����ȷ�����Դ�ѡC��
�����Ѷȣ�һ��
3��ѡ���� X��Y��Z��W��R���Ƕ�����Ԫ�أ�������Ԫ�����ڱ��е����λ����ͼ��ʾ������W����������ϼ���������ϼ۾���ֵ��ȣ�����˵����ȷ���ǣ�������
A��X��Y�γɵ�ij�ֻ��������Ϊ���������X2����Դ
B��Z��W��R�ֱ���X�γɵĻ������ˮ���ﶼ��ǿ��
C����̬�⻯������ȶ��ԣ�HmX��HmR��WHn
D��������YmX��YmR�У������Ӱ뾶�����������Ӱ뾶
�ο��𰸣�W����������ϼ���������ϼ۾���ֵ��ȣ���������ϼ���������ϼ۾���ֵ֮��һ������8������W��λ�ã���֪W�裬ZΪAl��YΪNa��RΪS��XΪO��
A��X��Y�γɵĻ������������ƺ������ƣ����й������ƿ��ԺͶ�����̼��ˮ��Ӧ��������������Ϊ��������Դ����A��ȷ��
B��Z��W��R�ֱ���X�γɵĻ������ˮ����Ϊ��Al��OH��3��H2SiO3��H2SO4�����Ƿֱ����ڼ���ᡢǿ�ᣬ��B����
C��O��S��Si�ĵõ�������˳��Ϊ��O��S��Si������̬�⻯������ȶ��ԣ�H2O��H2S��SiH4����C��ȷ��
D���ڻ����������ƺ������У������Ӱ뾶С�������Ӱ뾶����D����
��ѡAC��
���������
�����Ѷȣ�һ��
4��ѡ���� ���л�ѧ������ȷ����
[? ]
A. ��ϩ�Ľṹ��ʽ��CH2CH2
B. �����ǵĽṹʽ��C6H12O6
C. Ca2+�Ľṹʾ��ͼ��
D. NH4Cl�ĵ���ʽ��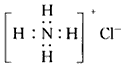
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ������Ԫ��A��B��C��D��ԭ���������ε��������ǵ�ԭ������֮��Ϊ32����ԭ������������֮��Ϊ10��A��Cԭ�ӵ�����������֮�͵���Bԭ�ӵĴ�����������A��C��B��D��Ϊͬ����Ԫ�أ�����������ȷ���ǣ�������
A��.����Ԫ�ص�ԭ�Ӱ뾶��A��B��C��D
B������������Ӧ��ˮ��������ԣ�B��D
C��CԪ�ش���Ԫ�����ڱ��е�3���ڵڢ�A��
D��C������������Ӧ��ˮ������ǿ��
�ο��𰸣�A��Cԭ�ӵ�����������֮�͵���Bԭ�ӵĴ�����������A��C��B��D��Ϊͬ����Ԫ�أ�B�Ĵ���������Ϊ8������A��C��������������Ϊ4��������Ԫ��A��B��C��D��ԭ���������ε���������AΪC��CΪSi��ԭ������������֮��Ϊ10������10-4-42=1����B��D��Ϊ�ڢ�A��Ԫ�أ�����BΪNa�����ǵ�ԭ������֮��Ϊ32��32-6-14-11=1������DΪH�����������⣻
��B�Ĵ���������ӦΪ2��A��C��Ϊ�ڢ�A��Ԫ�أ���ԭ������������֮��Ϊ10������10-1-12=4������B��D��Ϊ�ڢ�A��Ԫ�أ�ԭ���������ε�������BΪC��DΪSi��AΪH��CΪNa��
A�����Ӳ�Խ�࣬�뾶Խ��ͬ���ڴ�������ԭ�Ӱ뾶�ڼ�С������ԭ�Ӱ뾶ΪC��D��B��A����A����
B���ǽ�����C��Si����������������Ӧ��ˮ��������ԣ�B��D����B��ȷ��
C��CԪ��ΪNaԪ�أ�����Ԫ�����ڱ��е�3���ڵڢ�A�壬��C����
D��C������������Ӧ��ˮ����ΪNaOH��Ϊǿ���D����
��ѡB��
���������
�����Ѷȣ�һ��