1��ʵ���� ������ʽ��ʾ��������ԭ��Ӧ���һ��ԭ��أ�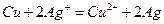
��1��װ�ÿɲ����ձ������ţ�������ԭ��ص�װ�ü�ͼ��
��ע��ԭ��ص�����������
��ע�����·�е��ӵ�����
��2��д�������缫�ϵĵ缫��Ӧ��
�ο��𰸣���1��(6��)
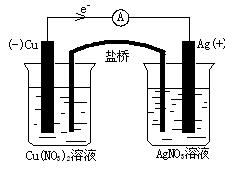 ?
?
(ѡ�������������Ϻ͵������Һ�������)
��2��(ÿ��2��)?������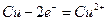 �� ������
�� ������ ��
��
�����������
�����Ѷȣ���
2������� ��1��������ͼװ�ã�����ģ�����ĵ绯ѧ��������XΪ̼����Ϊ�������ĸ�ʴ������KӦ������_____������XΪп������K����M�����õ绯ѧ��������Ϊ____________________��
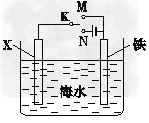
��2���£�N2H4���ֳ���������һ�ֿ�ȼ��Һ�壬��ȼ���Ƚϴ���ȼ�ղ���Ի�������Ⱦ���ʿ����������ȼ�ϡ��¡�����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20����30����KOH��Һ���õ�طŵ�ʱ��ͨ���µ�һ��Ϊ______�����ü��ĵ缫��Ӧʽ��______________________________����ع���һ��ʱ��������Һ��pH ��________�����������С���������䡱����
��3���ⱻ��Ϊ������Ԫ�ء�����ѧ�����ز����ɷ�ֹ��ȱ�����������(KIO3)�ǹ��ҹ涨��ʳ�μӵ�������ľ���Ϊ��ɫ��������ˮ������������Խ���������������⻯�����þ����ɵ��ʵ⡣�Ե�Ϊԭ�ϣ���ͨ������Ʊ�����ء����������������ö��Ե缫�����������������������ӽ���Ĥ��������ش��������⣺
�ٵ��ǰ���Ƚ�һ�����ľ��Ƶ����ڹ�������������Һ���ܽ�ʱ������Ӧ��3I2+6KOH=5KI+KIO3+3H2O��������Һ��������������������������Һ������������������ˮ��ȴ�����ʱ�������Ϸ�����Ӧ�ĵ缫��ӦʽΪ_________________________________��
�ڵ������У�Ϊȷ������Ƿ���ɣ��������Һ���Ƿ���I-�������һ��������Һ���Ƿ���I-��ʵ�鷽��������Ҫ����д�±���Ҫ������ҩƷֻ�ܴ������Լ���ѡ��ʵ�������������Ʒ��ѡ���Լ���������Һ���⻯�ص�����ֽ������������Һ��ϡ���ᡣ?
�ο��𰸣���1��N����������������������
��2��������N2H4 + 4OH����4e����N2�� + 4H2O����С
��3����2I-��2e-��I2?��I-��6e-��6OH-��IO3-��3H2O��?
��
���������
�����Ѷȣ�һ��
3������� ��13�֣���1����п��ͭ�õ������Ӻ����2mol/L��ϡ�����У������缫��ӦʽΪ_________________������ ��Ӧ����������ԭ�������Ӵ� �����·�� ����п��ͭ������Һ��H+ �� �ƶ���������������
��2�����ݷ�Ӧ2Fe3+ + Cu = 2Fe2++Cu2+ ���ԭ��أ����踺������Ϊ ����Һ��Fe3+�� �������������������Ǩ�ƣ�������ӦʽΪ ��������ӦʽΪ ��
�ο��𰸣���1��2H++2e-=H2�� ��ԭ п ͭ ����
��2��Cu������ Cu-2e-=Cu2+ 2Fe3+ +2e- = 2Fe2+
�����������1����п��ͭ�õ������Ӻ����2mol/L��ϡ�������γ�ԭ��أ���ԭ�����п�Ǹ���������������Ӧ��ͭ����������Һ�е������ӵõ�������������������ԭ��Ӧ���缫��ӦʽΪ2H++2e-=H2�������·�ϣ����ӴӸ����ص��ߵ��������������Ǵ�п�����·��ͭ����Һ��H+ �������ƶ�����2�����ݷ�Ӧ2Fe3+ + Cu = 2Fe2++Cu2+ ���ԭ��أ�ͭ�Ļ��ϼ���0������Ϊ+2�ۣ�����������Ӧ����ԭ��صĸ������缫��ӦʽΪCu-2e-=Cu2+���������Һ��������Fe3+������Ǩ�ƣ��������Ϸ�����ԭ��Ӧ���缫��ӦʽΪ2Fe3+ +2e- = 2Fe2+��
���㣺����ԭ���ԭ�����缫����ʽ��д��
�����Ѷȣ�һ��
4������� ��ͼ�е������ҺΪ����ͭ��Һ����Fe�缫��______�������������������ͬ������缫��ӦʽΪ______���÷�Ӧ��______�����������ԭ������ͬ����Ӧ��Cu�缫��______����缫��ӦʽΪ______���÷�Ӧ��______��Ӧ��
���ȼҵ�ϣ����ö��Ե缫��ⱥ���Ȼ�����Һ�Ƶ��������ռ��缫��Ӧʽ�ֱ�Ϊ������______����______���ܵĵ�ط�ӦʽΪ______��
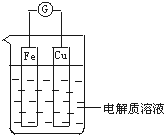
�ο��𰸣��ٸ�ԭ����У�������������������ʧ���������������Ӷ�����������Ӧ���缫��ӦʽΪFe-2e-�TFe2+��ͭ��������������ͭ���ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪCu2++2e-�TCu��
�ʴ�Ϊ��������Fe-2e-�TFe2+��������������Cu2++2e-�TCu����ԭ��
���ö��Ե缫��ⱥ���Ȼ�����Һʱ��������������ʧ���ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H++2e-=H2����������������ʧ���ӷ���������Ӧ���缫��ӦʽΪ2Cl--2e-=Cl2�����ڵ�ʧ������ͬ�����£����������缫��Ӧʽ��Ӽ��õ�ط�Ӧʽ�����Ե�ط�ӦʽΪ2NaCl+2H2O���.H2��+Cl2��+2NaOH��
�ʴ�Ϊ��2H++2e-=H2����2Cl--2e-=Cl2����2NaCl+2H2O���.H2��+Cl2��+2NaOH��
���������
�����Ѷȣ���
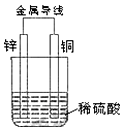
5��ѡ���� ������ͼ��ʾװ�õ���������ȷ����
[? ]
A���������пƬһ���ƶ�?
B��ͭƬ��������
C��������пƬ����������ͭƬ?
D����������ͭƬ���汻��ԭ
�ο��𰸣�AD
���������
�����Ѷȣ���