1、选择题 卤族元素随着原子序数的增大,下列递变规律正确的是
A.单质熔、沸点逐渐降低
B.单质的氧化性逐渐增强
C.原子半径逐渐增大
D.气态氢化物稳定性逐渐增强
参考答案:C
本题解析:同主族自上而下原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱,相应氢化物的稳定性也逐渐减弱,所以选项C正确,BD错误。卤素单质的熔沸点自上而下是逐渐升高的,A是不正确。答案选C。
本题难度:简单
2、填空题 在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1mol XY2含有54 mol电子。
(1)该融雪剂的化学式是_______________;X与氢元素形成的化合物的电子式是______________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
_______________;D与E能形成一种非极性分子,该分子的结构式为_______________;D所在族元素的氢化物中,沸点最低的是_______________。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是_______________。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与水反应的化学方程式为___________________。
参考答案:(1)CaCl2;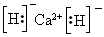
(2) ;S=C=S;H2S
;S=C=S;H2S
(3)Si3N4
(4)2F2+2H2O==4HF+O2
本题解析:
本题难度:一般
3、选择题 已知X为ⅠA族元素,Y为ⅥA族元素,则X、Y形成化合物的化学式不可能为
A.X2Y
B.X2Y2
C.XY2
D.XY3
参考答案:D
本题解析:
本题难度:一般
4、选择题 根据元素在周期表中的位置判断,下列元素中原子半径最小的是
A.氧
B.氟
C.碳
D.氮
参考答案:B
本题解析:同周期自左向右原子半径逐渐减小,四种元素都是第二周期元素,氟的原子序数增大,原子半径最小,所以答案选B。
本题难度:困难
5、简答题 短周期元素X、Y、Z、W原子序数依次增大.X是形成化合物种类最多的元素,Y是自然界含量最多的元素,Z是同周期中金属性最强的元素,W的负一价离子与Y的某种氢化物分子含有相同的电子数.
(1)元素X、Y、Z按原子半径由大到小的顺序排列为______.(用元素符号表示).
(2)W的单质与水反应的离子方程式为______.
(3)化合物A由X、Y、Z三元素共同构成,其浓溶液中通入W的单质时,可产生气体XY2和化合物ZWY3.反应的化学方程式为______.
参考答案:X是形成化合物种类最多的元素,应为C元素,Y是自然界含量最多的元素,应为O元素,Z是同周期中金属性最强的元素,应为Na元素,W的原子序数比Z大,应为第三周期元素,且W的负一价离子与Y的某种氢化物分子含有相同的电子数,应为Cl元素,则
(1)X为C,Y为O,Z为Na,C和O位于同一周期,原子半径C>O,Na位于第三周期,原子半径最大,则原子半径顺序为Na>C>O,故答案为:Na>C>O;
(2)W为Cl,单质与水发生:Cl2+H2O=H++Cl-+HClO,故答案为:Cl2+H2O=H++Cl-+HClO;
(3)化合物A由C、O、Na三元素共同构成,其浓溶液中通入Cl的单质时,可产生气体CO2和化合物NaClO3,说明A为碳酸盐,应为Na2CO3,反应的化学方程式为3Cl2+3Na2CO3=5NaCl+NaClO3+3CO2,故答案为:3Cl2+3Na2CO3=5NaCl+NaClO3+3CO2.
本题解析:
本题难度:一般