1、选择题 在一定条件下,将物质的量相同的NO和O2混和,发生如下反应:2NO+O2=2NO2,2NO2 N2O4,所得混合气体中NO2的体积百分含量为40%,此时,混合气体的平均分子量为
N2O4,所得混合气体中NO2的体积百分含量为40%,此时,混合气体的平均分子量为
A.49.6
B.41.3
C.62
D.31
参考答案:A
本题解析:略
本题难度:一般
2、选择题 将等物质的量的A、B混合于2 L的密闭容器中,发生下列反应:
3A(g)+B(g) ?xC(g)+2D(g),经4min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.125mol・L-1・min-1,下列说法正确的是
?xC(g)+2D(g),经4min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.125mol・L-1・min-1,下列说法正确的是
A.反应速率v(B)=0.13 mol・L-1・min-1
B.该反应方程式中,x=1
C.4min时,A的物质的量为0.75mol
D.4min时,A的转化率为50%
参考答案:D
本题解析:根据题意得v(D)=0.5mol/L/4min=0.125 mol・L-1・min-1,以C表示的平均速率v(C)=0.125mol・L-1・min-1,根据化学反应速率之比等于方程式中化学计量数之比的x=2,B错误;同理可计算出v(B)=1/2v(D)=0.0625 mol・L-1・min-1,A错误;4min时,D的物质的量是0.5mol/L×2 L=1mol,所以消耗A、B的物质的量分别是1.5mol、0.5mol,设AB的起始物质的量均为ymol,则剩余A、B的物质的量分别是y-1.5mol、y-0.5mol,根据c(A):c(B)=3:5,得(y-1.5)/( y-0.5)=3:5,解得y=3mol。所以4min时,A的物质的量为3-1.5=1.5mol,C错误;A的转化率为1.5mol/3mol×100%=50%,D正确,答案选D。
本题难度:一般
3、计算题 在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应。各物质的起始加入量如下:A、B和C均为4.0mol,D为6.5mol,F为2.0mol,设E为x mol。当x在一定范围内变化时,均可通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器正中位置。请填写以下空白:

(1)若x=4.5,则右侧反应在起始时向________________(填“正反应”或“逆反应”)方向进行。欲使起始反应维持向该方向进行,则x的最大取值应小于________________。
(2)若x分别为4.5和5.0,则在这两种情况下,当反应平衡时,A的物质的量是否相等?________________(填“相等”、“不相等”或“不能确定”)。其理由是________________。
参考答案:(1)正反应;7.0。
(2)不相等;因为这两种情况是在两种不同温度下达到化学平衡,平衡状态不同,所以物质的量也不同。
本题解析:题中给出一个容积固定的反应器,虽然中间有一个移动隔板,但题中要求隔板处于反应器的正中位置,也就是要求反应容器左右两侧反应的物质的量始终相等。要满足这一条件,①可通过投入E的物质的量即x值的大小来控制;②可通过温度的调节来实现。
(1)反应器左侧的反应为一个反应前后总体积不变化的反应,总物质的量始终为nA+nB+nC=4mol+4mol+4mol=12mol,这就要求反应器右侧也必须始终保持总的物质的量也为12mol。当x=4.5时,右侧反应在起始时总的物质的量为6.5mol+4.5mol+2mol=13mol,大于12mol,此时反应向总体积缩小的方向移动,即向正反应方向进行。由于右侧的正反应是一个体积缩小的反应,E物质参与反应的越多,体积缩小的越多。用极限法,假设投入的E物质全部反应,即E的最大投入量,也就是x的最大取值,则
D(g) + 2E(g)  2F(g)
2F(g)
n始(mol) 6.5 x 2.0
n平(mol) 6.5-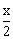 0 2.0+x
0 2.0+x
因左侧反应混合物总的物质的量为12mol,所以达平衡时,右侧反应需满足:
6.5-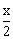 +0+2.0+x=12,x=7
+0+2.0+x=12,x=7
(2)若x分别为4.5和5.0这两种情况时,要满足题中移动隔板恰好处于反应器正中位置的要求,即反应器右侧在z值不同时还始终保持总物质的量为12mol,只有通过条件①即调节温度来实现。也就是说当x的取值在4.5和5.0这两种情况下,当隔板恰处中间位置时的温度是不相同的。再来分析反应器的左侧。由右侧的条件决定x的数值不同,温度不同,在不同的温度下平衡状态不同,各物质的量也就不同。故A的物质的量在这两种情况下也不相等。
本题难度:一般
4、计算题 将相同物质的量的SO3充入下面的两个容器中,已知甲容器有活塞可以上下移动,乙容器体积固定,在相同的温度、压强下开始发生反应:2SO3(g) ?2SO2(g)+O2(g),在反应过程中维持体系温度不变。
?2SO2(g)+O2(g),在反应过程中维持体系温度不变。
(1)求达到平衡状态时SO3气体的转化率的大小关系?
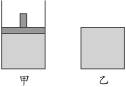 图2-2
图2-2
(2)达到平衡状态时分别充入一定量的Ar气,平衡是否会移动?会怎样移动?
参考答案:(1)甲容器中SO3的转化率比乙容器中SO3的转化率要大
(2)甲容器平衡向正反应方向移动,SO3的转化率增大,乙容器平衡不移动
本题解析:开始时两个容器中SO3的物质的量、体积、温度都是相等的,而且在反应过程中维持温度不变,即两个容器的温度始终是相同的,由于反应是一个气体分子数目增多的反应,所以对于乙容器来说,随着反应的不断进行其压强会逐渐增大,而甲容器随着气体分子数目的增多,活塞会逐渐向上移动,其体积会逐渐增大,所以乙容器相当于在A容器的基础上进行加压,而对于可逆反应2SO3(g) ?2SO2(g)+O2(g),加压会使得平衡向逆反应方向移动,这样会使转化率减小,所以达到平衡状态时甲容器中SO3的转化率比乙容器中SO3的转化率要大。
?2SO2(g)+O2(g),加压会使得平衡向逆反应方向移动,这样会使转化率减小,所以达到平衡状态时甲容器中SO3的转化率比乙容器中SO3的转化率要大。
当两个容器中都达到平衡状态后,再分别充入一定量的Ar气,乙容器由于体积没有改变,反应体系中各种物质的浓度并没有变化,正、逆反应速率仍然相等,所以其平衡不会移动。甲容器由于活塞的移动会导致体积增大,三种物质的浓度同等倍数减小,这和直接将活塞向上提一样,所以这时的情况相当于压强减小,其平衡向正反应(气体分子数目增多)方向移动,SO3的转化率要增大。
本题难度:简单
5、选择题 在一恒容的容器中充入2mol A和1mol B,发生反应2A(g)+B(g) xC(g),达到平衡后,C的体积分数为W%。若维持容器中的容积和温度不变,按起始物质的量:A为0.6mol,B为0.3mol,C为1.4mol充入容器,达到平衡后,C的体积分数仍为W%,则x的值为
xC(g),达到平衡后,C的体积分数为W%。若维持容器中的容积和温度不变,按起始物质的量:A为0.6mol,B为0.3mol,C为1.4mol充入容器,达到平衡后,C的体积分数仍为W%,则x的值为
[? ]
A.只能为2
B.只能为3
C.可能是2,也可能是3
D.无法确定
参考答案:C
本题解析:
本题难度:一般