1、选择题 青苹果汁遇碘溶液显蓝色,熟苹果能还原新制的氢氧化铜浊液,这说明
A.青苹果中只含淀粉不含糖类
B.苹果转熟时淀粉水解为单糖
C.熟苹果中只含糖类不含淀粉
D.苹果转熟时单糖聚合成淀粉
参考答案:B
本题解析:青苹果汁遇碘溶液显蓝色说明其中含有淀粉,熟苹果能还原新制的氢氧化铜浊液,说明含有单糖,但并没有说熟苹果汁遇碘溶液不显蓝色,青苹果不能还原新制的氢氧化铜浊液,所以A、C说法是不准确的,而D是明显错误的.本题实验与淀粉水解实验中检验淀粉的水解程度类似.要证明淀粉已完全水解,应取水解后的溶液少许,加碘水,若溶液不变蓝色,说明水解后的溶液中已不含淀粉,即淀粉已完全水解;若要证明淀粉未水解,应取水解后的溶液少许,先加碱中和,再加新制的氢氧化铜浊液后加热至沸腾,无红色沉淀出现;若要证明淀粉已部分水解,则既要用碘水证明水解液中有淀粉,又要用新制的氢氧化铜浊液(或银氨溶液)证明水解液中含还原糖.
本题难度:一般
2、选择题 以下叙述不正确的是
A.在水中氢、氧原子间的作用力只有共价键
B.金属和非金属化合既可能形成离子键,也可能形成共价键
C.离子键是阴、阳离子之间的静电吸引和静电排斥共同作用的结果
D.H2、Cl2反应,首先H2、Cl2分子的共价键断裂成H、Cl原子,而后H、Cl间形成离子键?
参考答案:AD
本题解析:A选项水分子内氢原子与氧原子间以化学键相结合,分子间H、O原子间存在氢键。D选项中氢、氯原子之间只形成共价键。
本题难度:一般
3、选择题 列各组微粒,不能互称为等电子体的是
A.NO2、NO2+、NO2-
B.CO2、N2O、N3-
C.CO32-、NO3-、SO3
D.N2、CO、CN-
参考答案:A
本题解析:价电子数和原子数分别都相等的是等电子体,A中价电子数不相等,其余都是的,答案选A。
本题难度:简单
4、选择题 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等。X、Y也是短周期主族元素,且X+、Y2-的核外电子排布相同。下列说法错误的是
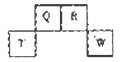
A.非金属性:Q B.Q、R、W三种元素的常见单质中所含微粒间的作用力完全相同
C.原子半径:X>T;离子半径:X+D.T单质能与X的最高价氧化物的水化物反应
参考答案:B
本题解析:结合四短周期元素Q、R、T、W的相对位置及“T所处的周期序数与主族序数相等”可推断出T元素为铝,进而可知Q、R、W分别为C、N、S元素;再根据Y2-所带电荷可判定Y为VIA元素,必为O,X则必为Na。
A.由S及C的最高价含氧酸的酸性硫酸大于碳酸,可知非金属性C<S,正确
B.C、N、S的常见单质分别为金刚石(石墨)、氮气、硫磺,微粒间的作用力分别为化学键、分子间力、分子间力。
C.微粒半径大小比较的规律是:电子层数越大半径越大,如果电子层数相同,核电荷数越大半径越小,故原子半径Na>Al,离子半径:Na+<O2-
D.铝可与钠的最高价氧化物的水化物NaOH反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑
故答案为B
本题难度:困难
5、选择题 下列每组物质发生状态变化所克服的微粒间的相互作用属同种类型是
A.食盐和蔗糖的熔化
B.白磷和硫的熔化
C.氯化铵固体和干冰受热后的气化
D.氧化镁和金属镁的熔化
参考答案:B
本题解析:A中克服的是离子键和分子间作用力,B中克服的都是分子间作用力,C中克服的是离子键、共价键和分子间作用力,D中克服的是离子键和金属键。所以答案是B。
本题难度:简单