1��ѡ���� ������������ܽ�ƽ���ƶ��ص���
A�����죬����ơ��ƿ������ð��������ĭ
B��ʵ�����У�����FeSO4��Һ���õ�����ˮ�����ü��ȵķ�����ȥ�ܽ���
C�������Ƽҵ�У�������������ƷNH4Cl֮ǰ������Һ�м���NaCl������ͨ������NH3
D�������У��ñ���̼������Һϴȥ����ư���ϵ����ۣ�������Һ��Ч������
�ο��𰸣�D
���������D�̼������Һ�ʼ��ԣ������ڼ�����Һ��ˮ��ij��ף�����û���漰����ѧƽ����ƶ�����ѡD��
���������⿼����ǻ�ѧƽ���ƶ������֪ʶ��ʹ��ѧƽ���ƶ���������Ҫ�У��¶ȡ�ѹǿ��Ũ�ȵȣ�ѧ��Ҫ����������������
�����Ѷȣ���
2��ѡ���� ���ܱ����з������з�ӦaA(g) 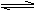 cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����
cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����
A��A��ת���ʱ�С
B��ƽ��������Ӧ�����ƶ�
C��D������������
D��a < c��d
�ο��𰸣�AD
����������������֪������ѹǿ������ƽ�ⲻ�ƶ���D��Ũ��Ϊԭƽ���2����������1.8������ƽ�����ơ�
A ��ȷ��A��ת���ʱ�С
B ����ƽ�����淴Ӧ�����ƶ�
C ����D�����������С
D ��ȷ������ѹǿ��ƽ�������������С�ķ����ƶ�����a < c��d
�����Ѷȣ�һ��
3��ѡ���� ��2NO2(����ɫ) N2O4(��ɫ)�Ŀ��淴Ӧ��,����״̬һ������ƽ��״̬����(����)��
N2O4(��ɫ)�Ŀ��淴Ӧ��,����״̬һ������ƽ��״̬����(����)��
A��N2O4��NO2�ķ�������Ϊ1��2
B��N2O4��NO2��Ũ�����
C��ƽ����ϵ����ɫ���ٸı�
D����λʱ������1 mol N2O4��ΪNO2��ͬʱ,��1 mol NO2��ΪN2O4
�ο��𰸣�C
�����������Ӧ�������ɫ���ٱ仯,˵��NO2Ũ�Ȳ���,��Ӧ�ﵽƽ�⡣
�����Ѷȣ�һ��
4��ѡ���� �ظ������Һ�д�������ƽ�⣺Cr2O72-(�Ⱥ�ɫ)+H2O  2H++2CrO42-(��ɫ)����K2Cr2O7��Һ�м������������Լ�����Һ��ɫ��ӻ�ɫ��Ϊ�Ⱥ�ɫ
2H++2CrO42-(��ɫ)����K2Cr2O7��Һ�м������������Լ�����Һ��ɫ��ӻ�ɫ��Ϊ�Ⱥ�ɫ
A��NaHSO4
B��NaHCO3
C��Na2CO3
D��CH3COONa
�ο��𰸣�A
�����������Һ�ӻ�ɫ��Ϊ�Ⱥ�ɫ����Ӧ������С�A��HSO4�C�Ƕ�Ԫǿ���������ˮ��Һ��ˮ�������ϴ�HSO4-=H++SO42-��ʹ��Һ��H+Ũ������Cr2O72-(�Ⱥ�ɫ)+H2O  2H++2CrO42-(��ɫ)���淴Ӧ������У�����Һ��Ϊ�Ⱥ�ɫ��B��HCO3-����Һ�в���ˮ��HCO3-+H2O
2H++2CrO42-(��ɫ)���淴Ӧ������У�����Һ��Ϊ�Ⱥ�ɫ��B��HCO3-����Һ�в���ˮ��HCO3-+H2O H2CO3+OH-,H2O
H2CO3+OH-,H2O H++OH-��C��CO32-��ˮ��Һ�в���ˮ�⣬��Һ��CO32-+H2O
H++OH-��C��CO32-��ˮ��Һ�в���ˮ�⣬��Һ��CO32-+H2O  HCO3?+OH-,H++OH-?
HCO3?+OH-,H++OH-? H2O����Ӧ������У�D��CH3COO-+H+
H2O����Ӧ������У�D��CH3COO-+H+ CH3COOH����Ӧ������С�
CH3COOH����Ӧ������С�
�����Ѷȣ�һ��
5��ѡ���� ��6�֣����������Һ�У��������µ���ƽ�⣺HF? H�� + F��
��1���������NaOH ,����ƽ����________��Ӧ�����ƶ�, c(H+)_______________��
��2���������NaF , ����ƽ����________��Ӧ�����ƶ� , c(H+)____________��
��3�������¶ȣ�����ƽ����__________��Ӧ�����ƶ���c��H+��_________________��
�ο��𰸣���6�֣�(1) ������С��(2) �棬��С (3)?��������
�����������1���������NaOH�����������ӣ���ƽ�������ƶ����������������ӣ���c(H+)��С��
��2���������NaF��������Ũ������ƽ�������ƶ���c(H+)��С��
��3��������ʵĵ������ȣ��������¶ȣ�����ƽ�������ƶ���c��H+������
�ʴ�Ϊ��(1) ������С��(2) �棬��С (3)?�� ������
�����Ѷȣ���