1��ѡ���� ���淴Ӧ��X(g)?+?2Y(g) 2Z(g)?����2M(g)
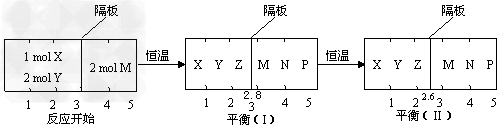
2Z(g)?����2M(g) N(g)?+?P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܷ���塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ�������ж���ȷ����
N(g)?+?P(g)�ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܷ���塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ�������ж���ȷ����
[? ]
A.?��Ӧ�ٵ��淴Ӧ�Ƿ��ȷ�Ӧ
B.?��ƽ�⣨I��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ14:15
C.?��ƽ�⣨I��ʱ��X��ת����Ϊ5/11
D.?��ƽ�⣨I����ƽ�⣨II����M������������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� 850��C�����´��ڿ��淴Ӧ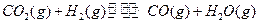 ���ﵽ�����ʱ��90%�����������������ת��Ϊˮ����֪�ڸ�״̬�´��ڹ�ϵ
���ﵽ�����ʱ��90%�����������������ת��Ϊˮ����֪�ڸ�״̬�´��ڹ�ϵ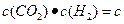
 �����������ж�����̼�������������Ϊ��?��
�����������ж�����̼�������������Ϊ��?��
A��1��1
B��5��1
C��9��1
D��10��1
�ο��𰸣�C
������������⿼�黯ѧƽ����㣻�跴Ӧǰ���������Ϊ1L����ת��������Ϊ0.9L������ƽ��״̬ʱ�������Ũ�ȱȿ�֪���ﵽƽ��ʱCO2�����Ϊ8.1L��ת����CO2Ϊ0.9L����ԭ�������CO2�����Ϊ9L��V(CO2):V(H2)=9:1��
�����Ѷȣ���
3��ѡ���� һ���¶��£��ڹ̶��ݻ������Ϊ2L���ܱ������г���1mol?N2��3mol?H2������Ӧ������Ӧ���е�10sĩʱ��Ӧ�ﵽƽ�⣬��ʱ������c��NH3��=0.1mol?L-1�������й��жϴ�����ǣ�������
A����Ӧ��ƽ��ʱN2��ת����Ϊ10%
B����Ӧ���е�10?sĩʱ��H2��ƽ����Ӧ������0.03?mol?��L?s��-1
C���÷�Ӧ�ﵽƽ��ʱ��N2��ƽ��Ũ��Ϊ0.45?mol/L
D���÷�Ӧ�ﵽƽ��ʱ��ѹǿ����ʼʱѹǿ��0.95��
�ο��𰸣����ݻ�ѧƽ�������ʽ��ʽ����
? ?N2+3H2=2NH3
��ʼ����mol��? 1? 3? 0
�仯����mol��?0.1? 0.3?0.2
ƽ������mol��?0.9?2.7?0.2
A����Ӧ��ƽ��ʱN2��ת����=0.1mol1mol��100%=10%����A��ȷ��
B��Ӧ���е�10?sĩʱ��H2��ƽ����Ӧ����=0.3mol2L10s��0.015mol?��L?s��-1 ����B����
C���÷�Ӧ�ﵽƽ��ʱ��N2��ƽ��Ũ��=0.9mol2L=0.45?mol/L����C��ȷ��
D���÷�Ӧ�ﵽƽ��ʱ��ѹǿ����ʼʱѹǿ֮�ȵ����������ʵ���֮�ȣ���0.9+2.7+0.2������1+3��=0.95����D��ȷ��
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ��X��Y��1�U2������Ȼ�Ϻ������ܱ������У���ѹ��3��107Pa���������·�Ӧ��X��g����2Y��g��
 2Z��g�����ﵽƽ��״̬ʱ����÷�Ӧ��������ʵ�����������������ʵ�����ȣ��й�������ͼ����Ӧ��Ӧ���¶���
2Z��g�����ﵽƽ��״̬ʱ����÷�Ӧ��������ʵ�����������������ʵ�����ȣ��й�������ͼ����Ӧ��Ӧ���¶���
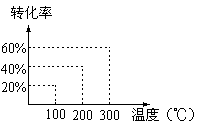
[? ]
A��100��
B��200��
C��300��
D������ȷ��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5������� 2A? B + C��ijһ�¶�ʱ���ﵽƽ�⡣
B + C��ijһ�¶�ʱ���ﵽƽ�⡣
(1)?���¶����ߣ�ƽ��������Ӧ�����ƶ���������Ӧ��_________��Ӧ������Ȼ����ȣ���
(2)?��BΪ���壬����ѹǿƽ�� ���淴Ӧ�����ƶ�����A��___________̬��
���淴Ӧ�����ƶ�����A��___________̬��
(3)?��A����̬ʱ����ѹʱ��ƽ�ⲻ�ƶ�����BΪ_________̬��CΪ__________̬��
(4) ��A��B��C��Ϊ���壬���������ƽ��___________�ƶ�(�� ��������)
��������)
�ο��𰸣���1��_����?��(2)? __��_______��(3)? BΪ__��__̬��CΪ__��__̬��(4) __��_
�����������
�����Ѷȣ�һ��