|
高考化学试题《物质结构和元素周期律》试题强化练习(2019年最新版)(六)
2019-06-25 21:00:39
【 大 中 小】
|
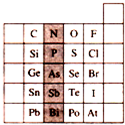
1、选择题 如图是元素周期表的一部分,关于图中阴影部分元素的说法中,正确的是( )
A.N元素为第一周期元素
B.PH3的稳定性比H2S强
C.该纵行元素的最高价氧化物对应的水化物化学式均为H3RO4
D.H3AsO4的酸性比H3PO4弱
| 
参考答案:A、N元素在元素周期表中第二周期,故A错误;
B、P的非金属性小于S的非金属性,则PH3的稳定性比H2S弱,故B错误;
C、该纵行元素的最高价氧化物对应的水化物化学式多为H3RO4,但N元素的最高价氧化物对应的水化物化学式多为HNO3,故C错误;
D、因非金属性As<P,则H3AsO4的酸性比H3PO4弱,故D正确;
故选D.
本题解析:
本题难度:一般
2、填空题 下表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题.
族
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0
二
⑥
⑦
三
①
③
⑤
⑧
四
②
④
⑨
|
(1)③④⑤三种元素金属性最强的是______(填元素符号),⑥⑦⑧三种元素所形成的气态氢化物最不稳定的是______.(填分子式)
(2)金属性最强的单质与水反应的化学方程式是______.
(3)由②⑥⑦三种元素形成的常见化合物的水溶液呈______性(填“酸”、“碱”、“中”),原因是:______(用离子方程式表示).
(4)我国首创的海洋电池以⑤单质为负极,铂网为正极,海水为电解质溶液,⑤单质与⑦单质反应产生电流,其正极反应式为:______.
(5)溶质为8.0g的①的最高价氧化物水化物的稀溶液和溶质为8.0g⑧的氢化物的稀溶液发生反应放出11.46kJ热量,则此反应的热化学方程式为______.
参考答案:由元素在周期表中的位置可知,①为Na,②为K,③为Mg,④为Ca,⑤为Al,⑥为C,⑦为O,⑧为Cl,⑨为Br,
(1)同周期随原子序数增大金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,故金属性Ca>Mg>Al,非金属性Cl>C、O>C,故氢化物中CH4最不稳定,
故答案为:Ca;CH4;
(2)上述元素中K的金属性最强,与水反应生成KOH与氢气,反应方程式为:2K+2H2O=2KOH+H2↑,
故答案为:2K+2H2O=2KOH+H2↑;
(3)由②⑥⑦三种元素形成的常见化合物为K2CO3,属于强碱弱酸盐,溶液中碳酸根水CO32-+H2O?HCO3-+OH-,破坏水的电离平衡,使溶液呈碱性,
故答案为:碱;CO32-+H2O?HCO3-+OH-;
(4)Al与氧气、海水构成原电池,正极发生还原反应,氧气在正极获得电子,中性条件下生成氢氧根,正极电极反应式为:O2+2H2O+4e-=OH-,
故答案为:O2+2H2O+4e-=OH-;
(5)由反应NaOH+HCl=NaCl+H2O,可知NaOH与HCl按质量之比为40:36.5进行反应,故8gNaOH与8gHCl反应时NaOH不足,NaOH完全反应,放出热量为11.46kJ,则1molNaOH反应放出的热量=11.46kJ×1mol×40g/mol8g=57.3kJ,故该反应热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ/mol,
故答案为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ/mol.
本题解析:
本题难度:简单
3、选择题 下列有关物质的结构或性质的叙述错误的是
A.H3BO3、H2CO3、HNO3的酸性逐渐增加
B.BeSO4、MgSO4、CaSO4、BaSO4的溶解性逐渐减弱
C.S2-、Cl-、K+、Ca2+的离子半径依次增大
D.NH3、PH3的水溶性依次降低
参考答案:C
本题解析:
本题难度:困难
4、推断题 具有相同电子层结构的A、B两种离子,可组成AB型离子化合物。A、B的单质在常温时都可与水剧烈反应。试推断: ?
(1)A离子的结构示意图________;B原子的结构示意图___________。 ?
(2)A单质与水反应的离子方程式为__________________。 ?
(3)B单质与水反应的化学方程式为__________________。
参考答案:(1)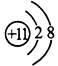 ; ;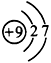
(2)2Na+2H2O=2Na++2OH-+H2↑?
(3)2F2+2H2O=4HF+O2
本题解析:
本题难度:一般
5、选择题 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。下列说法正确的是

[? ]
A.元素Z位于元素周期表中第3周期第ⅠA族
B.原子半径的大小顺序为:rW>?rZ?>rY>?rX
C.Y、W元素的氢化物,其化学式都为H2R
D.离子Y2-和Z3+的核外电子数和电子层数都相同
参考答案:D
本题解析:
本题难度:简单
| 