1��ѡ���� ��������Ϊ100 g��Cu���缫�����AgNO3��Һ���Ե��һ��ʱ����������������28 g����ʱ�����������ֱ�Ϊ
A������100 g������128 g
B������91.0 g������119.0 g
C������93.6 g������121.6 g
D������86.0 g������114.0 g
�ο��𰸣�C
���������������֪����Cu�ܽ⣬����Ag���������ܽ��Cu������Ϊx����
Cu��2Ag
64? 2��108
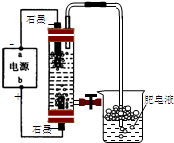
x?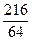 x
x
100+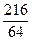 x-(100-x)=28,x=6.4
x-(100-x)=28,x=6.4
�����Ѷȣ���
2��ѡ���� �ò����缫�����һ��Ũ�ȵ��������ʵ�ˮ��Һ������������ʣ����Һ�м�����ˮ����ʹ��Һ�͵��ǰ��ͬ���ǣ�������?
A��AgNO3
B��H2SO4?
C��NaOH
D��NaCl?
�ο��𰸣�A�����AgNO3����������Ag����������O2��Ҫʹ��Һ�ָ���ԭ����Ũ�ȣ�Ӧ����Ag2O����A����
B��������ᣬ����������������������������ʵ��Ϊ���ˮ���������ˮ�ɻָ���ԭ����Ũ�ȣ���B��ȷ��
C�����NaOH������������������������������ʵ��Ϊ���ˮ���������ˮ�ɻָ���ԭ����Ũ�ȣ���C��ȷ��
D�����ʳ��ˮ������NaOH��H2��Cl2����������Ȼ���ָܻ����ǰ��״̬��Ӧͨ��������HCl���壬��D����
��ѡBC��
���������
�����Ѷȣ���
3��ѡ���� ���������������Ϊ26.0%�ı���ʳ��ˮ100g��ͨ��0.200mol���Ӻ���Һ��NaOH����������������ֵ�ǣ�������
A��8.02%
B��8.00%
C��8.63%
D��8.61%
�ο��𰸣���ⱥ���Ȼ�����Һ��������������ʧ���ӷ���������Ӧ���������������������ӵõ����ӷ�����ԭ��Ӧ���������������еķ�ӦΪ2NaCl+2H2O?ͨ��?.?2NaOH+H2��+Cl2������Ӧ��ת�Ƶ���2mol��������������Ϊ2mol������0.5mol������0.5mol��ͨ��0.200mol���Ӻ�������������Ϊ0.2mol������0.1mol������0.1mol�����Ե�����Һ��NaOH����������������ֵ=0.2mol��40g/mol100g-0.1mol��2g/mol-0.1mol��71g/mol��100%=8.63%
��ѡC��
���������
�����Ѷȣ�һ��
4������� ��ҵ��Ϊ�˴�������Cr2O72-���Թ�ҵ��ˮ����������Ĵ�������������ҵ��ˮ��������NaCl����FeΪ�缫���е�⣬����һ��ʱ�䣬��Cr(OH)3��Fe(OH)3�������ɣ���ҵ��ˮ�и��ĺ����ѵ����ŷű�����ش��������⣺
?��1������������Ӧ�ĵ缫��Ӧʽ��������______________ ��������______________ ��
?��2��д��Cr2O72-��ΪCr3+���ӷ���ʽ��_______________________ ��?
?��3����ˮ�����Ա�Ϊ���Ե�ԭ����_____________________________ ��
?��4��________(��ܡ����ܡ�)����ʯī�缫��ԭ����_________________ ��
�ο��𰸣�
��1��Fe�D2e-��Fe2+��2H+��2e-��H2��
��2��Cr2O72-��6Fe2+��14H+ ��2Cr3+��6Fe3+��7H2O
��3��H+�����������ϵõ��ӳ�ΪH2����������Cr2O72-��Fe2+�ķ�ӦҲ������H+��ʹ����Һ���Ա�Ϊ���ԣ��������Ա�Ϊ���ԣ�Cr3+��3OH-��Cr(OH)3��, Fe3+��OH-��Fe(OH)3��
��4�����ܣ�������ʯī�缫����������ΪCl2��������Fe2+��û��Fe2+�Ļ�ԭ���ã� Cr2O72-�Ͳ��ܱ�ΪCr3+��Ҳ�Ͳ���ת����Cr(OH)3����������ȥ��
���������
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��ijѧ�������ļ��û���������Һ�����������������ǵ��з�̪�ı���ʳ��ˮ��ͨ�������Ӻ����������д�����ǣ�������
A����ȼ�ŵ�ľ���ȼ�������е���������б�����
B���Ӳ������зų�������Һ����Ҫ�ɷ���NaClO?��?NaCl
C�����Դa�������ĵ缫������Һ����ɫ�仯��ɫ����ɫ����ɫ
D�����Դb�������ĵ缫�ϲ���������������