| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《电解池原理》高频试题预测(2019年最新版)(十)
参考答案:B 本题解析:加入0.1 mol Cu(OH)2后恰好恢复到电解前的浓度,Cu(OH)2从组成上可看成CuO?H2O,根“析出什么加入什么”的原则知,析出的物质是氧化铜和水,则阴极上析出氢气和铜,生成0.1mol铜转移电子个数=0.1mol×2×NA/mol=0.2NA,根据原子守恒知,生成0.1mol水需要0.1mol氢气,生成0.1mol氢气转移电子的个数=0.1mol×2×NA/mol=0.2NA,所以电解过程中共转移电子数为0.4NA,阴极上析出氢气和铜,A错误;B、阴极上析出氢气和铜,生成0.1mol铜转移电子个数=0.1mol×2×NA/mol=0.2NA,根据原子守恒知,生成0.1mol水需要0.1mol氢气,生成0.1mol氢气转移电子的个数=0.1mol×2×NA/mol=0.2NA,所以电解过程中共转移电子数为0.4NA,故B正确;C、加入0.1 mol Cu(OH)2后恰好恢复到电解前的浓度,说明硫酸铜的物质的量为0.1mol,溶液的体积未知,故硫酸铜的浓度未知,C错误;D、阳极电极反应是氢氧根离子失电子生成氧气的过程,阳极反应式是4OH--4e-=2H2O+O2↑,故转移0.4mol电子,生成0.1mol氧气,体积为2.24L,D错误;答案选B. 本题难度:一般 2、选择题 1L0.1mol・L―1 AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是(设电解按理论进行,溶液不蒸发)? (? ) 参考答案:C 本题解析:本电解槽的阴阳极反应为: 本题难度:简单 3、选择题 用惰性电极和串联电路电解下列物质的水溶液:①NaCl?②NaNO3?③CuCl2?④AgNO3,在相同时间内生成气体的总体积(同温同压下测定),理论上从多到少的顺序是( ) 参考答案:电解时,氯化钠溶液中氯离子和氢离子放电,硝酸钠溶液中氢离子和氢氧根离子放电,氯化铜溶液中氯离子和铜离子放电,硝酸银溶液中氢氧根离子和银离子放电. 本题解析: 本题难度:简单 4、选择题 下列有关说法正确的是 |
参考答案:C
本题解析:A.将0.2mol/L的NH3・H2O与0.1mol/L的HCl溶液等体积混合后生成氯化铵,其中氨水过量,且二者的浓度相等。溶液的pH >7,说明氨水的电离程度大于铵根的水解程度,则c(NH4+)>c(Cl-)>c(OH-)>c(H+),A错误;B.已知MgCO3的Ksp=6.82×10-6,但所有含有固体MgCO3的溶液中,不一定有C(Mg2+)=C(CO32-),且c(Mg2+)・c(CO32-)==6.82×10-6 mol?L―1,B错误;C.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合后根据物料守恒可知: 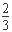 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),C正确;D.用惰性电极电解Na2SO4溶液,相当于是电解水,阳阴两极产物分别是氧气和氢气,则二者物质的量之比为1:2,D错误,答案选C。
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),C正确;D.用惰性电极电解Na2SO4溶液,相当于是电解水,阳阴两极产物分别是氧气和氢气,则二者物质的量之比为1:2,D错误,答案选C。
考点:考查溶液中离子浓度比较、溶度积常数应用以及电解原理的应用等
本题难度:一般
5、实验题 (16分)如下图所示装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。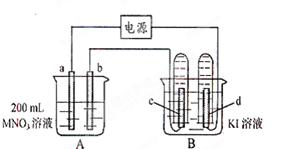
试回答:
(1)a为?极,c极的电极反应式为: ?。
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶液,你能观察到的现象是?
? ?
? 。电解进行一段时
。电解进行一段时
间后,罩在c极上的试管中 也收集到了气体,此时c极上的电极反应式为:?。
也收集到了气体,此时c极上的电极反应式为:?。
(3)当d电极上收集到44.8 ml气体(标准状况)时停止电解,a极上放出了?mol气体,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为 ?。若要使A池中溶液恢复原浓度,应加?。
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200 ml,取这种溶液加入到25.0 ml? 0.100 mol・L-1的HCl溶液中,当加入31.25 ml 溶液时刚好沉淀完全。由此可知电解前A烧杯中MNO3 溶液的物质的量浓度为?mol・L-1。
溶液的物质的量浓度为?mol・L-1。
参考答案:
本题解析:略
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《物质结构和元素周.. | |