1、简答题 如图所示的电解装置中,乙池盛有20OmL饱和CuSO4溶液,丙池盛有2OOmL饱和NaCl溶液.通电一段时间后,C极增重0.64g,则:
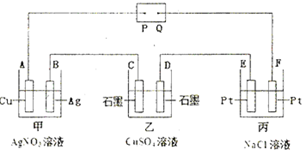
(1)P是电源的______极.
(2)甲池中,A极的质量______(填“增加”或“减少”)______g.电解一段时间,甲池溶液的pH______(填“变大”、“变小”或“不变”).
(3)D极的电极反应式为______,丙池电解反应的离子方程式为______,相同状况下,D电极与E电极产生的气体体积比为______.
(4)电解后,乙、丙电池中溶液的pH分别为乙______、丙______(设溶液体积不变,温度为室温,也不考虑溶液的水解).
(5)若乙池溶液通电一段时间后,向所得的溶液中加入0.1mol的Cu(OH)2后恰好恢复到电解前的浓度.则电解过程中转移电子的数目为______.(用NA表示)
参考答案:(1)乙池盛有20OmL饱和CuSO4溶液,C极增重0.64g,则C极发生Cu2++2e-=Cu,即C极为阴极,由图可知,P为负极,故答案为:负;
(2)甲中A电极发生Ag++e-=Ag,则A电极质量增加,由Cu~2e-~2Ag,则Ag的质量为0.64g64g/mol×2×108g/mol=2.16g,硝酸银溶液的浓度不变,则pH不变,
故答案为:增加;2.16;不变;
(3)乙中D为阳极,发生的电极反应为4OH--4e-=2H2O+O2↑,丙中发生2NaCl+2H2O?电解?.?2NaOH+H2↑+Cl2↑,其离子反应为2Cl-+2H2O?电解?.?2OH-+H2↑+Cl2↑,E电极为氢气,
由电子守恒可知O2~2H2,则D电极与E电极产生的气体体积比为1:2,
故答案为:4OH--4e-=2H2O+O2↑;2Cl-+2H2O?电解?.?2OH-+H2↑+Cl2↑;1:2;
(4)由电子守恒可知,乙中Cu~H2SO4,则c(H+)=0.01mol×20.2L=0.1mol/L,其pH=1;由电子守恒可知丙中Cu~2NaOH,则c(OH-)=0.01mol×20.2L=0.1mol/L,其pH=13,
故答案为:1;13;
(5)乙池溶液通电一段时间后,向所得的溶液中加入0.1mol的Cu(OH)2后恰好恢复到电解前的浓度,发生2CuSO4+2H2O?电解?.?2Cu+O2↑+2H2SO4、2H2O?电解?.?2H2↑+O2↑,
由Cu(OH)2?△?.?CuO+H2O,则转移的电子数为(0.1mol×2+0.1mol×2)×NA=0.4NA,故答案为:0.4NA.
本题解析:
本题难度:一般
2、选择题 高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:
Ni(OH)2+M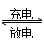 NiOOH+MH,下列叙述正确的是
NiOOH+MH,下列叙述正确的是
A.放电时正极附近溶液的碱性增强
B.放电时负极反应为:M+H2O+e-===MH+OH-
C.放电时阳极反应为:NiOOH+H2O+e-===Ni(OH)2+OH-
D.放电时每转移1 mol电子,正极有1 mol NiOOH被氧化
参考答案:A
本题解析:放电相当于原电池,C不正确。正极是得到电子的,根据总反应式可知,正极是NiOOH中的Ni得到电子被还原,生成Ni(OH)2,碱性增强,A正确,D不正确。原电池中负极失去电子,因此选项B不正确。答案选A。
本题难度:一般
3、填空题 (6分)利用碳棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当碳棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗。试计算:
(1)锌片的质量减少了多少?
(2)原稀硫酸溶液的物质的量浓度。
(3)有多少个电子通过了导线。
参考答案:⑴ 9.75g?⑵ 0.75mol/L?⑶ 1.806×1023
本题解析:略
本题难度:简单
4、选择题 镍氢电池比碳锌或碱性电池有更大的输出电流,更适合用于高耗电产品。镍氢电池的总反应式是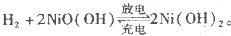 。下列叙述错误的是
。下列叙述错误的是

A.电池充电时,氢元素被还原
B.电池放电时,镍元素被氧化
C.电池放电时,氢气在负极反应
D.电池放电时,电池负极周围溶液的碱性减弱
参考答案:B
本题解析:A、电池充电时,H元素的化合价降低发生还原反应,正确;B、电池放电时,Ni元素的化合价降低,发生还原反应,错误;C、电池放电时,氢气发生氧化反应,所以在电池的负极被氧化,正确;D、结合C选项,氢气发生氧化反应生成氢离子,与电解质溶液中的氢氧根离子结合生成水,所以电池负极周围溶液的碱性减弱,正确,答案选B。
本题难度:一般
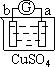
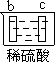
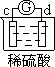
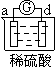
5、选择题 有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置
| 
| 
| 
| 
|
部分实验现象
| a极质量减小
b极质量增加
| b极有气体产生
c极无变化
| d极溶解
c极有气体产生
| 电流计指示在导线中
电流从a极流向d极
|
由此可判断这四种金属的活动性顺序是
A.a>b>c>d? B.b>c>d>a? C.d>a>b>c? D.a>b>d>c
参考答案:C
本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。a极质量减小,b极质量增加,这说明a电极是负极,失去电子,b电极是正极,溶液中的铜离子得到电子,则金属性是a>b。b电极有气体产生,c极无变化,这说明b的金属性强于c的;d极溶解,c极有气体产生,这说明d电极是负极,c电极是正极,溶液中的氢离子放电,生成氢气,则金属性是d>c;电流计指示在导线中电流从a极流向d极,这说明d电极是负极,a电极是正极,则金属性是d>a,所以这四种金属的活动性顺序是d>a>b>c,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。主要是考查对原电池原理,以及灵活运用原电池判断金属性强弱的熟悉了解程度,旨在培养学生分析、归纳和总结问题的能力。该题的关键是明确原电池的工作原理,然后结合题意和装置图灵活运用即可。
本题难度:一般