1、实验题 (5分)某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:

2、填空题 多晶硅是太阳能光伏产业的重要原料。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
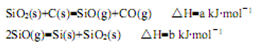
①反应SiO2(s)+2C(s)=Si(s)+2CO(g)的△H=?kJ・mol-1(用含a、b的代数式表示)。
②SiO是反应过程中的中间产物。隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式是?。
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g) Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;
Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;

①X是?(填“H2”、“SiHCl3”)。
②上述反应的平衡常数K(1150℃)?K(950℃)(选填“>”、“<”、“=”)
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
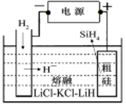
①用粗硅作原料,熔盐电解法制取硅烷原理如图10,电解时阳极的电极反应式为?。
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为?。
3、填空题 铅蓄电池是化学电源,其电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O根据上述情况判断
(1)蓄电池的负极是______,其电极反应式为______。
(2)蓄电池的正极是______,其电极反应式为______。
(3)蓄电池工作时,其中电解质溶液的pH______(增大、减小、不变)。
4、填空题 (14分)1773年,伊莱尔・罗埃尔(Hilaire Rouelle)发现尿素。1828年,弗里德里希・维勒首次使用无机物质氰酸钾[KCNO]与硫酸铵人工合成了尿素[CO(NH2)2]。
(1)维勒合成尿素的化学反应方程式为?。
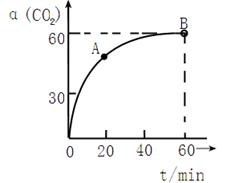
(2)工业上尿素是由CO2和NH3在一定条件下合成,其反应方程式为?当氨碳比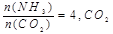 的转化率随时间的变化关系如图1所示。
的转化率随时间的变化关系如图1所示。
①A点速率v逆(CO2)?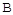 点速率为V正(CO2)(填“大于”、“小于”或“等于”)
点速率为V正(CO2)(填“大于”、“小于”或“等于”)
②NH3的平衡转化率为?。

(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图2。
①电源的负极为?(填“A”或“B”)。
②阴极室中发生的电极反应式为?
③电解结束后,阴极室溶液的pH与电解前相比将?(填“增大”、“减小”、“不变”)若两极共收集到气体11.2L(标准状况),则除去的尿素为??g(忽略气体的溶解)。
5、选择题 A、B、C都是金属:B中混有C时,只有C能被盐酸溶解;A与B与稀硫酸组成原电池时,A为电池的正极。A、B、C三种金属的活动性顺序为?
[? ]
A.A>B>C
B.A>C>B
C.C>B>A
D.B>C>A