1��ѡ���� ��ҵ�����е����������������Ⱦ����Ҫ��Դ��Ϊ���ۣ���ҵ��ͨ��ͨ��NH3��֮�������з�Ӧ��NOX+NH3��N2+H2O������NO��NO2�Ļ����3L������ͬ��ͬѹ�µ�3.5LNH3ǡ��ʹ����ȫת��ΪN2����ԭ���������NO��NO2�����ʵ���֮��( ? )
A��1��3
B��2��1
C��1��1
D��1��4
�ο��𰸣�A
���������
�����Ѷȣ���
2��ѡ���� ʢ��12mL?NO2��O2�Ļ���������Ͳ������ˮ���У���ַ�Ӧ��ʣ��2mL��ɫ���壬��ԭ���������O2������ǣ�������
A��1.2mL
B��2.4mL
C��3.6mL
D��4.8mL
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� �������ǵ����ػ�������ƽ�����ȼ�������ҷ�Ӧ������������������ӻ��β��������˸���������Ҫ��CO2��H2O��N2��NO����Щ�����Ϊ��ɫ���������Ƿ����ֳ������������������̣��������̵�ԭ����
[? ]
A��������N2����������NO2
B��NO����������NO2
C��CO2��NO��Ӧ����CO��NO2
D��NO��H2O��Ӧ����H2��NO2
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� ����˵������ȷ���ǣ�������
A����������������������Ũ����
B��K��ˮ��Ӧ��Li��ˮ��Ӧ����
C��CO��NO���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ�����
D��NO2��������ˮ���ռ�
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5������� ȼú�����������еĵ�������NOx����ҪΪNO��NO2�����γ���Ⱦ�����뾭�ѳ���������ŷţ�
��1���û�ѧ����ʽ��ʾNO�γ�����������ķ�Ӧ______
��2�������ѳ��������ʺܶ࣬����˵����ȷ����______
a����?H2O���ѳ��������������պ��������е�NO
b����?Na2SO3���ѳ�����O2�ή��Na2SO3��������
c����CO���ѳ�������ʹ������NO2��Ũ������
��3������[CO��NH2��2]��һ������������Ч��NOxת��ΪN2��
����֪��ͨ�����з����ϳ����أ�
2NH3��g��+CO2��g��?H2NCOONH4��s����H=-159.5kJ/mol
H2NCOONH4��s��?CO��NH2��2��s��+H2O��l����H=+28.5kJ/mol
�������ͷų�NH3���Ȼ�ѧ����ʽ��______
��д�������������ͷ�NH3��������˵������______
��CO��NH2��2��ij����������ҪΪN2��NO��O2���е�NO�����ʵ�����ֵ�ֱ�Ϊ1��2��2��1��3��1ʱ��NO�ѳ������¶ȱ仯��������ͼ��
������a?��ӦCO��NH2��2?��NO�����ʵ�����ֵ��______��
������a��b��c�У�800�桫900�������ڷ�����Ҫ��Ӧ�Ļ�ѧ����ʽ��______��
��900�桫1200���������ѳ����½���NOŨ����������������Ҫ��Ӧ��______��
������a�У�NO����ʼŨ��Ϊ6��10-4?mg/m3����A�㵽B�㾭��0.8s����ʱ�����NO���ѳ�����Ϊ______?mg/��m3?s����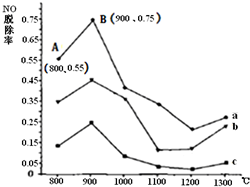
�ο��𰸣���1��һ���������ȶ�����������Ӧ���ɶ�������������������ˮ��Ӧ���������һ����������NO�γ�����������ķ�ӦΪ��2NO+O2�T2NO2��3NO2+H2O�T2HNO3+NO���ʴ�Ϊ��2NO+O2�T2NO2��3NO2+H2O�T2HNO3+NO��
��2��a��һ�������������ڣ�����������������ˮ����Ӧ����NO�����������պ��������е�NO����a��ȷ��
?b���������Ʋ��ȶ����ױ�����������O2�ή��Na2SO3�������ʣ���b��ȷ��
C����CO���ѳ���������������������õ��ӷ�����ԭ��Ӧ����������NO2��������NO2��Ũ�Ȳ����ӣ���c����
�ʴ�Ϊ��ab��
��3������֪��2NH3��g��+CO2��g��?H2NCOONH4��s����H=-159.5kJ/mol
H2NCOONH4��s��?CO��NH2��2��s��+H2O��l����H=+28.5kJ/mol
���ݸ�˹���ɣ����Ȼ�ѧ����ʽ��ӵ�2NH3��g��+CO2��g��?CO��NH2��2��s��+H2O��l����H=-131kJ/mol��
�������ͷų�NH3���Ȼ�ѧ����ʽΪ��CO��NH2��2��s��+H2O��l��?2NH3��g��+CO2��g����H=+131kJ/mol��
�ʴ�Ϊ��CO��NH2��2��s��+H2O��l��?2NH3��g��+CO2��g����H=+131kJ/mol��
���ͷŰ����ķ�Ӧ�����ȷ�Ӧ�������¶ȣ�������ƽ�������ȷ�Ӧ������У�ͬʱ�¶����ߣ��������ܽ�Ƚ��ͣ������������ͷŰ����ķ�����У�
�ʴ�Ϊ�������¶ȣ������¶�������ƽ�������ȷ�Ӧ������У�ͬʱ�¶����ߣ��������ܽ�Ƚ��ͣ������������ͷŰ����ķ�����У�
��CO��NH2��2?�ĺ���Խ�ߣ�NO��ת����Խ��NO�ѳ���Խ�ߣ���������a?��ӦCO��NH2��2?��NO�����ʵ�����ֵ��3��1���ʴ�Ϊ3��1��
��800�桫900��������NO�ѳ�����������NO����Ϊ��Ӧ��μӷ�Ӧ������ʱ�����طֽ����ɰ�����������̼��������һ����������������ԭ��Ӧ���ɵ�������������NO��Ӧ����N2��ͬʱ���ɶ�����̼��ˮ�����Է�Ӧ����ʽΪ��4NH3+6NO�T5N2+6H2O?��?2CO��NH2��2+6?NO�T2CO2+4H2O+5N2��
�ʴ�Ϊ��4NH3+6NO�T5N2+6H2O?��?2CO��NH2��2+6?NO�T2CO2+4H2O+5N2��
��900�桫1200���������ѳ����½�������NOŨ����������÷�Ӧ��Ӧ����NO�����طֽ����ɵİ����������е�������Ӧ����һ��������ˮ������NOŨ���������Է�Ӧ����ʽΪ��4NH3+5O2�T4NO+6H2O��
�ʴ�Ϊ��4NH3+5O2�T4NO+6H2O��?
��A�㵽BNO�ѳ�����0.55��Ϊ0.75����NO��Ũ�ȱ仯��Ϊ��0.75-0.55����6��10-4?mg/m3=1.2��10-4?mg/m3
����NO���ѳ�����=1.2��10-4mg/m30.8s=1.5��10-4mg/��m3��s����
�ʴ�Ϊ��1.5��10-4��
���������
�����Ѷȣ�һ��