1、简答题 在一个密闭容器中,发生下列反应:CO2(g)+C(s)?2CO(g)△H>0,达到平衡后,改变下列条件,则指定物质的浓度及平衡怎样变化?
(1)增加C,平衡______,c(CO)______.
(2)减小密闭容器的容积,保持温度不变,则平衡______,c(CO2)______.
(3)通入N2,保持密闭容器的容积和温度不变,则平衡______,c(CO2)______.
(4)保持密闭容器的容积不变,升高温度,则平衡______,c(CO)______.
参考答案:(1)加C是固体不影响平衡,化学平衡不动,一氧化碳浓度不变;
故答案为:不移动;不变;
(2)减小密闭容器的容积,保持温度不变,增大体系压强,平衡向气体体积减小的方向进行,平衡逆向进行,二氧化碳浓度增大;
故答案为:向逆反应方向移动;增大;
(3)氮气是惰气加入氮气,保持密闭容器的容积和温度不变,体系总压增大,气体分压不变,平衡不动,物质浓度不变;
故答案为:不移动;不变
(4)CO2(g)+C(s)?2CO(g)△H>0,反应是吸热反应,升温平衡正向进行,一氧化碳浓度增大;
故答案为:向正反应方向移动;增大;
本题解析:
本题难度:一般
2、选择题 下列有关反应限度的说法错误的是
[? ]
A.可逆反应达到限度之前逆反应速率逐渐增大与生成物浓度逐渐增大有关
B.炼铁高炉尾气中CO含量不随高炉高度改变而改变,是因为有关反应达到了限度
C.化学反应的限度决定了反应物在该条件下的最大转化率
D.可逆反应的限度不随反应条件的改变而改变
参考答案:D
本题解析:
本题难度:一般
3、选择题 一定量混合气体在密闭容器中发生如下反应:xA?+ yB(g)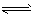 zC(g),达平衡后测得A气体的浓度为0.50 mol/L。恒温下将容器体积扩大1倍,反应重新达到平衡,测得A浓度为0.20mol/L。下列叙述中正确的是
zC(g),达平衡后测得A气体的浓度为0.50 mol/L。恒温下将容器体积扩大1倍,反应重新达到平衡,测得A浓度为0.20mol/L。下列叙述中正确的是
[? ]
A.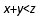
B.平衡向左移动
C.B的转化率减少
D.C的体积分数降低
参考答案:A
本题解析:
本题难度:一般
4、填空题 液化石油气中常存在少量有毒气体羰基硫(COS),必须将其脱除以减少环境污染和设备腐蚀。完成下列填空。
(1)写出羰基硫的电子式 ,羰基硫分子属于 (选填“极性”、“非极性”)分子。
(2)下列能说明碳与硫两元素非金属性相对强弱的是 。
a.相同条件下水溶液的pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
(3)羰基硫在水存在时会缓慢水解生成H2S,对钢铁设备产生电化学腐蚀。写出正极的电极反应式 ,负极的反应产物为 (填化学式)。
为除去羰基硫,工业上常采用催化加氢转化法,把羰基硫转化为H2S再除去:COS + H2 CO + H2S
CO + H2S
(4)已知升高温度,会降低羰基硫的转化率。则升高温度,平衡常数K ,反应速率 (均选填“增大”、“减小”、“不变”)。
(5)若反应在恒容绝热密闭容器中进行,能说明该反应已达到平衡状态的是 。
a.容器内气体密度保持不变 b.容器内温度保持不变
c.c(H2)=c(H2S) d.υ(H2)正=υ(H2S)正
(6)已知该反应的平衡常数很大,说明 。
参考答案:(1) , 极性 (各1分,共2分)
, 极性 (各1分,共2分)
(2)a c (2分)
(3)H2S + 2e → H2↑+S2-(或2H+ + 2e → H2↑)(2分) FeS(1分)
(4)减小,增大(各1分,共2分)
(5)b (2分)
(6)正反应进行程度很大(1分。其他合理答案也给分)
本题解析:(1)羰基硫相当于是二氧化碳中的1个氧原子被硫原子取代,所以其电子式为 。S和O的非金属性不同,所以该化合物是极性分子。
。S和O的非金属性不同,所以该化合物是极性分子。
(2)a.非金属性越强,最高价氧化物对应水化物的酸性越强,相应的钠盐水解程度越小,所以相同条件下水溶液的pH:Na2CO3>Na2SO4可以碳与硫两元素非金属性相对强弱,a正确;b.非金属性越强,最高价氧化物对应水化物的酸性越强,亚硫酸不是最高价含氧酸,所以酸性:H2SO3>H2CO3不能说明碳与硫两元素非金属性相对强弱,b不正确;c.CS2中碳元素为+4价,硫元素为-2价,说明非金属性是硫强于碳,c正确,答案选ac。
(3)原电池中负极失去电子发生氧化反应,正极得到电子发生还原反应,硫化氢分子中氢元素得到电子,发生还原反应,因此电极反应式为H2S + 2e → H2↑+S2-。负极铁失去电子,生成亚铁离子与硫离子结合生成硫化亚铁,所以负极产物是FeS。
(4)升高温度,会降低羰基硫的转化率,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应。则升高温度,平衡常数K减小,而反应速率增大。
(5)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,则a.密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此容器内气体密度始终保持不变,不能说明反应达到平衡状态,a不正确;b.由于反应在恒容绝热密闭容器中进行,所以容器内温度保持不变可以说明反应达到平衡状态,b正确;c.平衡时浓度不再发生变化,但物质的浓度之间不一定相等,故c(H2)=c(H2S) 不能说明反应达到平衡状态,c不正确;d.υ(H2)正=υ(H2S)正,但二者的反应速率方向相同,所以不能说明反应达到平衡状态,d不正确,答案选b。
(6)平衡常数越大,反应物的转化率越大,因此若该反应的平衡常数很大,说明正反应进行程度很大。
考点:考查非金属性强弱比较、原电池原理、外界条件对平衡状态以及有关平衡常数的应用
本题难度:困难
5、填空题 甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和反应②,用CH4和H2O为原料来制备甲醇(CH3OH).
①CH4(g)+H2O(g)?CO(g)+3H2(g)△H1
②CO(g)+2H2(g)?CH3OH(g)△H2
将0.20mol?CH4和0.30mol?H2O(g)通入容积为10L的密闭容器中,在一定条件下发生①反应,达到平衡时,CH4的转化率与温度、压强的关系如图.
(1)温度不变,缩小体积,增大压强,①的反应速率______(填“增大”、“减小”或“不变”),平衡向______方向移动.
(2)反应①的△H1______0(填“<”、“=”或“>”).
(3)如果反应①达到平衡时所用的时间为2min,求CH4的反应速率及化学平衡常数的值.(写出计算过程).
(4)在100℃压强为0.1MPa条件下,将a?mol?CO与?3a?mol?H2的混合气体在催化剂作用下进行②反应,生成甲醇.为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.请在下表空格中填入剩余的实验条件数据.
| 实验编号 | T(℃) | n?(CO)/n(H2) | P(MPa)
I
150
0.1
II
5
III
350
5
|

参考答案:(1)温度不变,缩小体积增大压强,反应速率增大,平衡向气体体积减小的方向移动,即反应①向逆反应移动,
故答案为:增大;逆反应;
(2)采取控制变量法分析,由图可知压强相同时,到达平衡时,温度越高CH4的转化率越大,升高温度平衡向正反应移动,故正反应为吸热反应,即△H>0,
故答案为:>;
(3)由100℃平衡CH4的转化率为0.5可知,消耗CH4为0.2mol×0.5=0.1mol,平衡时甲烷的浓度变化量为0.1mol10L=0.01mol/L,故v(CH4)=0.01mol/L2min=0.005mol/(L?min);
平衡时甲烷的浓度变化量为0.1mol10L=0.01mol/L,则:
?CH4(g)+H2O(g)?CO(g)+3H2(g)
开始(mol/L):0.02?0.03?0? 0
变化(mol/L):0.01? 0.01? 0.01? 0.03
平衡(mol/L):0.01? 0.02? 0.01? 0.03
故100℃时平衡常数k=0.033?×0.010.02×0.01=1.35×10-3,
答:CH4的反应速率为0.005mol/(L?min);100℃时平衡常数化学平衡常数的值为1.35×10-3;
(4)通过“控制变量法”探究外界条件对化学平衡的影响,探究的前提只能是改变一个条件,而其它条件不变,由此可得:Ⅱ中温度为150℃,n?(CO)/n(H2)为13,Ⅲ中n?(CO)/n(H2)为13,
故答案为:实验编号T(℃)n?(CO)/n(H2)P(MPa)III15013III13.
本题解析:
本题难度:一般