1、实验题 如图在试管A中先加入2mL的甲,并在摇动下缓缓加入2mL乙,充分摇匀,冷却后再加入丙,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管B中加入5ml丁溶液,按图连接好装置,用酒精灯对试管A小火加热3~5min后,改用大火加热,当观察到B试管中有明显现象时停止实验。试回答:

(1)写出下列物质的化学式(不用指出浓度)
甲?乙?
丙?丁?
(2)甲物质所含官能团的名称为?
(3)写出试管A中发生反应的化学方程式
?
(4)若用18O标记乙醇中的氧元素,则18O会出现在哪种生成物中??
(5)试管甲中加入浓硫酸的主要目的是?
(6)B中长导管不宜伸入试管的溶液中,原因是?
(7)B中使用丁溶液的作用是?
参考答案:(1)CH3CH2OH,H2SO4,CH3COOH,Na2CO3
(2)羟基
(3)乙醇与乙酸的酯化反应(条件1分,可逆符号1分,其余2分,共4分)
(4)乙酸乙酯
(5)催化剂(多答不扣分)
(6)防倒吸
(7)反应乙酸,溶解乙醇,降低乙酸乙酯的溶解度? (此空3分)
(没有作说明的每空2分)
此答案仅供参考
本题解析:略
本题难度:简单
2、选择题 下列每组物质只用水就能鉴别的一组是( )
A.苯、乙醇、四氯化碳
B.乙醇、乙醛、溴乙烷
C.乙醛、丙醇、硝基苯
D.硝基苯、乙醇、甘油
参考答案:A
本题解析:只用水就能鉴别,说明利用的是物质的溶解性。苯、四氯化碳、溴乙烷、硝基苯都是不溶于水的,其中苯的密度小于水的,而其余都是大于水的。乙醇、乙醛、丙醇和甘油都是和水互溶或易溶的,所以答案选A。
本题难度:简单
3、选择题  (2008年上海卷,化学,18)设计学生试验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见右图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸出)。下列气体的制取宜使用该装置的是
(2008年上海卷,化学,18)设计学生试验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见右图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸出)。下列气体的制取宜使用该装置的是
A.用二氧化锰(粉末)与双氧水制氧气
B.用锌粒与稀硫酸制氢气
C.用硫化亚铁(块状)与盐酸制硫化氢
D.用碳酸钙(块状)与稀硫酸制二氧化碳
参考答案:B

本题解析:利用启普发生器的原理,进行创新应用。本题考查启普发生器的应用的注意事项,从而考查了实验基本操作。选项A中二氧化锰为粉末状物质,关闭K时,反应不能停止;选项B中Zn为颗粒状物质,关闭K可以使试管内的气体压强增大,能达到反应停止;选项C中与选项B相似,但H2S有毒,对空气造成污染;选项D中CaCO3与H2SO4反应生成CaSO4,由于CaSO4微溶于水,附在CaCO3表面,使反应停止,达不到制取CO2的目的。
本题难度:简单
4、实验题 醛可与NaHSO3饱和溶液发生加成反应,生成水溶性的α-羟基磺酸钠:
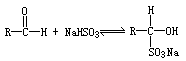
反应是可逆的。在通常条件下有70%~90%的原料向正反应方向转化。
(1)若氯苯中含有杂质苯甲醛,要除去此杂质,可作用的试剂是____,反应的化学方程式为:____;分离的方法是____。
(2)若使CH3―CHOH―SO3Na转化为乙醛,可采用的试剂是____,反应的化学方程式为____,分离的方法是____。
参考答案:
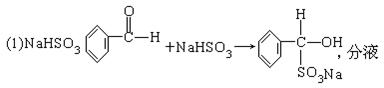
(2)H2SO4? 2NaHSO3+H2SO4==Na2SO4+2H2O+2SO2↑蒸馏
本题解析:充分应用题给信息,并联想有关化学平衡移动的概念和物质的性质分析题目要求。
(1)氯苯中混有苯甲醛,按题给反应,用NaHSO3与苯甲醛加成,生成可溶于水的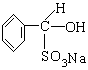 ,则与不溶于水的氯苯分为两层,用分液漏斗分离即可。反应的化学方程式为:
,则与不溶于水的氯苯分为两层,用分液漏斗分离即可。反应的化学方程式为:
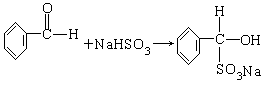
(2)注意到题给条件“反应是可逆的,在通常条件下”正反应方向的转化率较高,若能使平衡左移,则可生成乙醛,而考虑平衡左移的方法,若以CH3―CHOH―SO3Na为纯液体,没有浓度的问题,则只应考虑使左侧NaHSO3浓度减小的办法,则可相应使用H2SO4,发生反应:
2NaHSO3+H2SO4==Na2SO4+2H2O+2SO2↑
使NaHSO3浓度减小,而使平衡左移,转化为乙醛:

注意到Na2SO4为离子晶体,熔沸点较高,而CH3CHO沸点仅为20.8℃,易挥发,所以用蒸馏的方法,则可分离出乙醛。
本题难度:一般
5、选择题 世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成生石灰;②在海水中加入生石灰,过滤,洗涤沉淀物;
③将沉淀物与盐酸反应,结晶、过滤;④在氯化氢热气流中加热晶体;⑤电解上述所得盐(熔融条件下)。 下列说法正确的是
A.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净
B.上述变化过程中包括了分解、化合、复分解、置换等四种反应类型
C.在氯化氢热气流中干燥晶体的目的是为了加快干燥速度
D.步骤⑤也可以采用电解该盐水溶液的方法
参考答案:A
本题解析:B项:无置换反应,故错;C项:目的应为防止镁离子水解,故错;D项:电解其盐溶液得不到Mg,故错。故选A。
点评:本题考查的镁的制备的相关知识,题目难度不大,注意利用好题中所给出的信息是解题的关键。
本题难度:简单