1、实验题 (12分)某学业生利用以下装置制备氨气,并完成氨气的喷泉实验。

请回答下列问题:
(1)装置A中发生反应的化学方程式?。
(2)装置B中所盛的试剂是?。
(3)如果将制备氨气和氨气喷泉组合为一整套实验,用字母表示接口的连接顺序:
(?)、(?)、C、(?)(?)(?)(?)(?)
(4)组装好装置,检查装置的气密性后,加入试剂关闭K3,打开K1?、K2给A装置试管进行加热。当?(填写现象)时,即烧瓶中氨气收满。
(5)装置E的作用?。
(6)请叙述引发该喷泉实验的操作过程?。
2、选择题 下列制备物质的设计中,理论上正确、操作上可行、经济上合理的是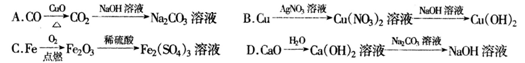
3、实验题 (10分)为了比较卤素单质的氧化性强弱,可在实验室先制取Cl2(利用MnO2与浓盐酸反应可制取Cl2),并将Cl2依次通入NaBr溶液和KI-淀粉溶液中。如图所示仪器及药品,试回答:

(1)若所制取气体从左向右流向时,上述仪器接口的连接顺序为________接________、________接________、________接________、________接________。(填字母)
(2)实验开始后装置5中反应的离子方程式为______________________________。
(3)装置3的作用是__________________________________,反应的离子方程式为_______________________________。
(4)装置1中产生的现象是:溶液先变蓝一段时间后蓝色褪去,生成两种强酸,请写出蓝色褪去的化学方程式:___________________________________________________。
4、实验题 (每空2分,共14分)
(一)用碳酸钠粉末配制0.2000 mol・L-1Na2CO3溶液0.5L
(1)需选用的玻璃仪器或用品?(填字母编号)
B、0.5L平底烧瓶? C、0.5L容量瓶? D、0.5L圆底烧瓶? E、烧杯? F、试管? G、胶头滴管? H、量筒? I、托盘天平? J、药匙? M、滤纸? N、玻璃棒
(2)应称取?g 碳酸钠粉末来溶于水
(二)用0.2000 mol・L-1Na2CO3溶液标定未知浓度的盐酸
(1)把0.2000 mol・L-1Na2CO3溶液装入?(酸式,碱式)滴定管中。从此滴定管中放出20. 00mL0.2000 mol・L-1Na2CO3溶液入锥形瓶中,滴2至3滴甲基橙作指示剂,用未知浓度的盐酸来滴定0.2000 mol・L-1Na2CO3溶液,根据?判断滴定终点达到。
00mL0.2000 mol・L-1Na2CO3溶液入锥形瓶中,滴2至3滴甲基橙作指示剂,用未知浓度的盐酸来滴定0.2000 mol・L-1Na2CO3溶液,根据?判断滴定终点达到。
(2)终点达到时,用去盐酸16.00mL(三次的平均值),则盐酸c(HCl)=?
(三)中和热的测定
用(二)实验中标定好浓度的盐酸50.0mL与0.55mol・L-1NaOH 50.0mL反应做中和热的测定实验。每次用量均一样,三次实验测得温 度升高的平均值为3.41℃,则实验测得中和热△H=?(混合后溶液的比热容C = 4.18J・℃-1・g-1),实验测得中和热比理论?(偏高,相等,偏低)
度升高的平均值为3.41℃,则实验测得中和热△H=?(混合后溶液的比热容C = 4.18J・℃-1・g-1),实验测得中和热比理论?(偏高,相等,偏低)
5、实验题 (4分)取三份锌粉,分盛于甲、乙、丙三支试管中,分别加入以下物质后,及时塞上导管塞子,充分反应。甲加入50mLpH=2盐酸,乙加入50mL pH=2醋酸,丙加入50mL pH=2醋酸及少量的胆矾粉末。
(1)若反应终了甲和乙中产生氢气的体积一样多,且只有一支试管中金属有剩余,则开始时加入的锌的质量大小关系为?(以上用“甲、乙”和? “>?、 < 、 ="”" 回答)
(2)若反应终了生成氢气的体积一样多,且没有剩余的锌。回答以下问题。
①三支试管中参加反应的锌的质量大小关系为:?
(用“甲、乙、丙”和? “>?、 < 、 ="”" 回答)
②反应终了,所需时间为:? (同①)
③若以上三组实验,锌粉均过量,产生的氢气体积?(同①)