1、选择题 下列仪器中,能直接加热的是?
A.烧杯
B.烧瓶
C.试管
D.容量瓶
参考答案:C
本题解析:试管能直接加热,烧杯和烧瓶要垫上石棉网加热,容量瓶不能加热,故选C。
点评:本题考查的是化学实验的基本常识,即化学仪器的使用,考查学生对各个化学仪器使用的熟悉程度。
本题难度:简单
2、选择题 下列有关试剂的保存方法正确的是
A.NaOH固体保存在配有橡皮塞的细口瓶中
B.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中
C.浓硫酸放在有软木塞的玻璃瓶中
D.Na2CO3溶液用容量瓶长期存放
参考答案:B
本题解析:略
本题难度:一般
3、选择题 实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是
[? ]
A.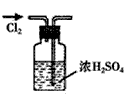
? 干燥Cl2
B.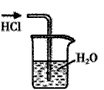
? 吸收HCl
C.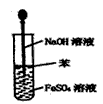
?制取Fe(OH)2沉淀
D.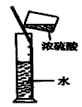
?稀释浓H2SO4
参考答案:C
本题解析:
本题难度:一般
4、实验题 海水中蕴藏着丰富的资源。海水综合利用的流程图如下。

(1)用NaCl做原料可以得到多种产品。
① 工业上由NaCl制备金属钠的化学方程式是_______________________________。
②电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:____________________________。
(2)分离出粗盐后的卤水中蕴含着丰富的镁资源,经过下列途径可获得金属镁:
卤水 Mg(OH)2
Mg(OH)2 MgCl2溶液→MgCl2・6H2O→MgCl2
MgCl2溶液→MgCl2・6H2O→MgCl2 Mg
Mg
其中,由MgCl2・6H2O制取无水MgCl2的部分装置(铁架台、酒精灯已略)如下:
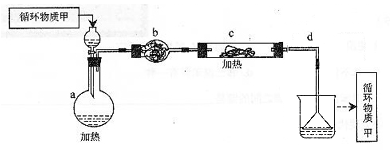
①上图中,装置a由?、?、双孔塞和导管组成。
②循环物质甲的名称是?。
③制取无水氯化镁必须在氯化氢存在的条件下进行,原因是?。
④装置b中填充的物质可能是?。
参考答案:(8分)(1) ① 2NaCl(熔融) 2Na+Cl2↑ (1分)
2Na+Cl2↑ (1分)
②NaCl+H2O NaClO+H2↑ (2分) (2) ① 分液漏斗、烧瓶?(2分)
NaClO+H2↑ (2分) (2) ① 分液漏斗、烧瓶?(2分)
② 盐酸 (1分)?③抑制晶体失水过程中的水解 (1分)?④氯化钙(1分)
本题解析:(1)①由于钠比较活泼,制取时只能采用电解熔融氯化钠的方法,反应的化学方程式为2NaCl(熔融) 2Na+Cl2↑。
2Na+Cl2↑。
②电解氯化钠溶液在阴极得到氢气,阳极得到氯气,同时还有氢氧化钠。生成的氯气被氢氧化钠溶液尾气吸收生成次氯酸钠即得到“84”消毒液,因此电解氯化钠溶液制取次氯酸钠的化学方程式为NaCl+H2O NaClO+H2↑。
NaClO+H2↑。
(2)①根据装置的结构特点可知,装置a是由分液漏斗、烧瓶、双孔塞和导管组成。
②MgCl2?6H2O在一定条件下加热得到无水MgCl2,若直接加热MgCl2?6H2O,会促进Mg2+水解,得不到无水MgCl2,因Mg2+水解呈酸性,加盐酸或在氯化氢气流中可抑制Mg2+水解,故一定条件为在HCl气流中,目的是抑制Mg2+水解,所以循环物质甲的名称是盐酸。
③根据以上分析可知,制取无水氯化镁必须在氯化氢存在的条件下进行,原因是抑制晶体失水过程中的水解。
④干燥管b中的物质是干燥氯化氢,由于氯化氢是酸性气体,所以b中填充的物质是氯化钙。
本题难度:一般
5、选择题 实验室中要配制1.00mol/L的Na2CO3溶液480 ml,配制时应选用的容量瓶的规格和称取的Na2CO3的质量分别是
A.480 ml ,50.9 g
g
B.500ml, 53.0g
C.500 ml, 53g
D.1000ml, 106.0g
参考答案:B
本题解析:略
本题难度:简单