1��ѡ���� ��һ�����Ľ����ƽ�������ʵ�飬��������������
[? ]
A������������������
B������������ˮ��
C������������ϡ������
D���ô���С���������ã���������ˮ��
�ο��𰸣�D
���������
�����Ѷȣ���
2��ѡ���� �����ʵ�����Fe��Mg��Al�ֱ������������ʵ���Ũ����ͬ��������ȫ��Ӧ����������������Ϊ��������
A��2��3��1
B��2��2��3
C��3��2��1
D��1��3��2
�ο��𰸣�Fe��Mg��Al�ֱ������ᷴӦ�ķ���ʽΪ��
Fe+2HCl�TH2��+FeCl2��
Mg+2HCl=MgCl2+H2����
Al+3HCl�T32H2��+AlCl3��
������þ���������ʵ����ֱ�Ϊ1mol�����ݷ�Ӧʽ��֪���ĵ���������ʵ����ֱ�Ϊ��2mol��2mol��3mol��
������������ʵ���֮��Ϊ��2��2��3�����ĵ�Ũ����������֮��ҲΪ2��2��3��
��ѡB��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ҵ������þ���ǽ�þ��������������ȴ������Ϊȴ������ǣ�?��
�ٿ���?��CO2?��Ar?��H2?��N2
A���٢�
B���ڢ�
C���ۢ�
D���ܢ�
�ο��𰸣�C
�����������
�����Ѷȣ���
4��ѡ���� ��һ��������Mg��Al�Ļ����Ͷ��500 mLϡ�����У�����ȫ���ܽⲢ�������壬����Ӧ��ȫ����������Һ�м���NaOH��Һ�����ɳ��������ʵ��������NaOH��Һ�������ϵ��ͼ��ʾ��������˵����ȷ���ǡ�(�� ��)��
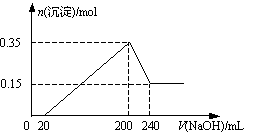 ?
?
A��Mg��Al��������Ϊ8 g
B����������ʵ���Ũ��Ϊ5 mol/L
C��NaOH��Һ�����ʵ���Ũ��Ϊ5 mol/L
D�����ɵ�H2�ڱ�״���µ����Ϊ11.2 L
�ο��𰸣�C
���������þ�����ֱ���ϡ���ᷴӦ��������þ���������Լ�����������ͼ���֪����������������Һ��û���������ɰ�ɫ��������˵��ϡ������ǹ����ġ��������������Ⱥ�����ϡ���ᷴӦ��Ȼ���ڷֱ�������þ����������Ӧ����������þ����������������������������Һ����ʱ�������������ܽ�������������Һ�У�����ƫ�����ƺ�ˮ������ͼ���֪��������������Ӧ����������ˮ240ml��200mol��40ml��������������0.35mol��0.15mol��0.20mol����˵������������0.2mol��������þ��0.15mol������þ�������ܵ�������0.15mol��24g/mol��0.2mol��27g/mol��9g����ϡ���ᷴӦ���ɵ�������0.3mol��0.15mol��0.45mol����״���µ������10.08L�����ݷ�ӦAl(OH)3��NaOH=NaAlO2��2H2O��֪���������Ƶ����ʵ���Ũ����0.2mol��0.04L��5.0mol/L����������ֵ�������������ǣ�0.2L��5mol/L����2��0.5mol������ϡ�����Ũ����0.5mol��0.5L��1.0mol/L����ѡC��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ����ע�ض�ѧ������֪ʶ������ѵ����ͬʱ�����ض�ѧ��������������ⷽ����ָ����ѵ��������Ĺؼ�����ȷ��Ӧ��ԭ����Ȼ���ٽ��ͼ��������ü��ɣ�����������ѧ����������������
�����Ѷȣ���
5��ʵ���� ���ʵ��̽����AlCl3��Һ�м��������NaOH����NaOH��Һ�м��������AlCl3�����Ƿ�һ����_________________________________
�ο��𰸣���AlCl3��Һ����μ���NaOH�а�ɫ�������ɣ���NaOH����ʱ�����ܽ⣬���������ΪNaAlO2����Ӧ�����ӷ���ʽΪ��Al3++3OH-==Al(OH)3����Al(OH)3+OH-==?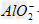 +2H2O
+2H2O
��NaOH��Һ����μ���AlCl3��Һʱ���۲쵽�������ǣ���ʼ�а�ɫ�������ɣ���������ʧ�������μ�AlCl3��Һֱ������ʱ���ֳ��ְ�ɫ�������Ҳ���ʧ��������Ϊ��Ӧ��ʼʱ������NaOH��Һ�����������AlCl3��NaOH����ת��ΪNaAlO2�����������AlCl3ʱ��AlCl3��NaAlO2����Һ�����Ӧ�����ɳ���Al(OH)3���䷴Ӧ�����ӷ���ʽΪ��Al3++3OH-====Al(OH)3����Al(OH)3+OH-==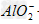 +2H2O��Al3++3
+2H2O��Al3++3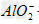 +6H2O==4Al(OH)3��
+6H2O==4Al(OH)3��
�������������ߵμ�˳��ͬ������һ����
���������
�����Ѷȣ�һ��