1、选择题 在两份体积相同的氢氧化钠和稀硫酸溶液中分别加入过量铝粉,充分反应后,在相同状况下,若放出氢气的体积相同,则该氢氧化钠溶液与硫酸溶液的物质的量浓度之比为( )
A.3:1
B.1:3
C.2:3
D.3:2
参考答案:令生成的氢气的物质的量为3mol,则:
2Al+3H2SO4=2Al2(SO4)3+3H2↑
3mol 3mol
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2mol 3mol
氢氧化钠和稀硫酸溶液的体积相等,所以所取氢氧化钠和稀硫酸溶液的浓度比等于溶质NaOH、H2SO4的物质的量的之比,即为2mol:3mol=2:3.
故选C.
本题解析:
本题难度:简单
2、填空题 某探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
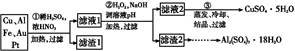
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为 ?。?
(2)第②步加H2O2的作用是 ?;?
调溶液pH的目的是使 生成沉淀。?
(3)用第③步所得CuSO4・5H2O制备无水CuSO4的方法是 。?
(4)由滤渣2制取Al2(SO4)3・18H2O ,探究小组设计了三种方案:
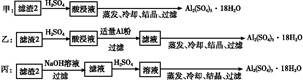
上述三种方案中, 方案不可行,原因是 ? ;?
从原子利用率角度考虑, 方案更合理。?
(5)探究小组用滴定法测定CuSO4・5H2O含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol /L EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2++H2Y2- CuY2-+2H+。写出计算CuSO4・5H2O质量分数的表达式w= ?;?
CuY2-+2H+。写出计算CuSO4・5H2O质量分数的表达式w= ?;?
下列操作会导致CuSO4・5H2O含量的测定结果偏高的是 ?。?
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子
参考答案:(1)Cu+2N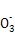 +4H+
+4H+ Cu2++2NO2↑+2H2O或3Cu+2N
Cu2++2NO2↑+2H2O或3Cu+2N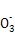 +8H+
+8H+ 3Cu2++2NO↑+4H2O(2分)
3Cu2++2NO↑+4H2O(2分)
(2)将Fe2+氧化为Fe3+(1分) Fe3+、Al3+(2分)
(3)加热脱水(2分)
(4)甲(2分) 所得产品中含有较多Fe2(SO4)3杂质(1分) 乙(2分)
(5)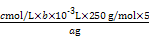 ×100% (2分)? c(2分)
×100% (2分)? c(2分)
本题解析:(1)铜和浓硝酸、稀硫酸的混合酸反应为:
开始发生:Cu+2N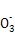 +4H+
+4H+ Cu2++2NO2↑+2H2O,
Cu2++2NO2↑+2H2O,
最后发生:3Cu+2N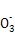 +8H+
+8H+ 3Cu2++2NO↑+4H2O;金属混合物中只有Au和Pt不溶于硝酸,故滤渣的主要成分是Au和Pt;(2)第②步加入H2O2的目的是将Fe2+氧化为Fe3+;H2O2氧化Fe2+时生成的是Fe3+和H2O,不引入杂质,对环境无污染;调整pH,使溶液中的Fe3+、Al3+转化为沉淀;(3)用第③步中所得的五水硫酸铜制取无水硫酸铜的方法是加热脱水;(4)滤渣2的主要成分是氢氧化铁和氢氧化铝,以此为基础分析该探究小组设计的三种方法,其中方案甲中制得的产品中一定含有较多的Fe2(SO4)3杂质;方案乙和丙中,从原子利用的角度考虑,乙方案最合理;(5)根据探究小组的方案,可知计算五水硫酸铜质量分数的表达式为:
3Cu2++2NO↑+4H2O;金属混合物中只有Au和Pt不溶于硝酸,故滤渣的主要成分是Au和Pt;(2)第②步加入H2O2的目的是将Fe2+氧化为Fe3+;H2O2氧化Fe2+时生成的是Fe3+和H2O,不引入杂质,对环境无污染;调整pH,使溶液中的Fe3+、Al3+转化为沉淀;(3)用第③步中所得的五水硫酸铜制取无水硫酸铜的方法是加热脱水;(4)滤渣2的主要成分是氢氧化铁和氢氧化铝,以此为基础分析该探究小组设计的三种方法,其中方案甲中制得的产品中一定含有较多的Fe2(SO4)3杂质;方案乙和丙中,从原子利用的角度考虑,乙方案最合理;(5)根据探究小组的方案,可知计算五水硫酸铜质量分数的表达式为:
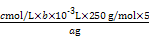 ×100%;滴定过程中,未干燥锥形瓶,对结果无影响,排除a;滴定终点时滴定管尖嘴中产生气泡,造成消耗EDTA的读数偏小,测定结果偏低,排除b;未除净干扰离子,造成EDTA消耗偏多,测定结果偏高,选c。
×100%;滴定过程中,未干燥锥形瓶,对结果无影响,排除a;滴定终点时滴定管尖嘴中产生气泡,造成消耗EDTA的读数偏小,测定结果偏低,排除b;未除净干扰离子,造成EDTA消耗偏多,测定结果偏高,选c。
本题难度:一般
3、选择题 由钠、镁、铝、铁四种金属中的两种组成的混合物12 g,与足量的盐酸反应,产生0.5 mol H2,则该混合物中一定不含(? )
A.Na
B.Mg
C.Al
D.Fe
参考答案:B
本题解析:该题是利用平均值进行的计算。由题意可知混合物可制得1 mol H2需要金属的质量是24 g,两种金属1 mol的质量应大于24 g和小于24 g,只有Mg制得1 mol H2需24 g,所以它不在混合物中(制得1 mol H2消耗Al的质量是18 g)。
本题难度:简单
4、填空题 某同学欲制取相同体积(同温同压)的氢气,他称取了两份铝粉,第一份加足量NaOH溶液,第二份加足量盐酸,则
(1)铝在元素周期表中的位置为______?其原子结构示意图为______
(2)涉及反应的离子方程式分别为______,______
(3)如果要得到相同体积(同温同压)的氢气,两份铝粉的质量比为______.
参考答案:(1)因铝的原子序数为13,所以其原子结构示意图为
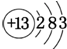
,所以在元素周期表中的位置为第三周期、第IIIA族;
(2)因铝粉与盐酸或氢氧化钠溶液反应,其化学方程式分别为:2Al+6HCl=2AlCl3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(3)因铝粉与盐酸或氢氧化钠溶液反应都能放出氢气:2Al+6HCl=2AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
由反应的化学方程式可以得知,相同条件下,等质量的铝分别跟足量的稀盐酸、NaOH溶液反应,放出氢气的质量都是3H2,因此,放出氢气的质量一样多.
故答案为:(1)第三周期 第IIIA族;
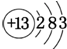
;
(2)2Al+6H+=Al3++3H2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)1:1
本题解析:
本题难度:一般
5、选择题 工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如图: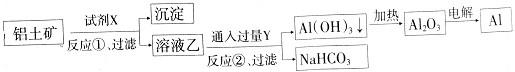
下列叙述不正确的是( )
A.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
B.反应①、过滤后所得沉淀为Fe2O3
C.图中所示转化反应都不是氧化还原反应
D.试剂X可以是氢氧化钠溶液
参考答案:A.反应①过滤后所得溶液乙为NaAlO2溶液,向NaAlO2溶液中通入过量CO2生成Al(OH)3沉淀,反应的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,故A正确;
B.Al2O3溶于氢氧化钠溶液得到NaAlO2溶液,Fe2O3与氢氧化钠溶液不反应,则过滤后所得沉淀为Fe2O3,故B正确;
C.电解熔融Al2O3属于氧化还原反应,故C错误;
D.试剂X可能是氢氧化钠等强碱溶液,可与氧化铝反应,故D正确.
故选C.
本题解析:
本题难度:简单