1、选择题 实验中要快速制取氢气,最好的方法是( )
A.纯锌和稀硫酸反应
B.纯锌和浓硫酸反应
C.粗锌和浓硫酸反应
D.粗锌(含铅铜杂质)与稀硫酸反应
2、实验题 (10分)某同学想利用镁与盐酸或醋酸在不同温度下反应,探究外界条件对反应速率的影响。部分实验用表如下:
实验
编号
| 温度/K
| 盐酸浓度
/mol・L-1
| 醋酸浓度/mol・L-1
| 实验目的
|
①
| 298
| 0.20
| ?
| a.实验①和②,探究温度对反应速率的影响;
b.实验①和③,探究浓度对反应速率的影响;
c.实验④⑤,探究温度对镁与盐酸反应和镁与醋酸反应速率的影响,哪个更大一些。
|
②
| 308
| 0.20
| ?
|
③
| 298
| 0.40
| ?
|
④
| ?
| 0.20
| 0.20
|
⑤
| ?
| ?
| ?
|
(1)请完成上工作表(填写实验④⑤的空格)。
(2)上表实验①中,镁条消失的时间为20s。实验过程中,镁条剩余质量与时间关系如图:
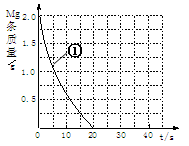
Ⅰ假设反应过程中盐酸体积不变,则要计算该反应的速率v(HCl),尚缺少的数据是???。
Ⅱ若反应温度每升高10℃,反应速率增大到原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的1/2,请在图中大致画出“实验②”、“实验④中醋酸实验”的镁条质量与时间关系曲线,并用②或④注明曲线代表的实验(假设实验中所用镁完全相同,且镁均能完全溶解)。
3、填空题 某同学探究外界条件对H2O2分解速率的影响,所用H2O2浓度为5%、10%,实验温度为20℃、40℃,其他试剂有1mol/LFeCl3溶液.每次实验H2O2的用量为2mL,FeCl3溶液2滴.
(1)请完成以下实验设计表:
| 实验编号 | 温度/℃ | H2O2浓度/% | 其它试剂 | 实验目的
①
20
5
无 | (Ⅰ)实验①和②探究催化剂对H2O2分解速率的影响;
(Ⅱ)实验②和③探究温度对该反应速率的影响;
(Ⅲ)实验②和④探究H2O2浓度对该反应速率的影响.
②
20
5
FeCl3溶液
③
______
______
______
④
______
______
______
|
(2)实验④产生气泡的速率比实验②快.分析引起反应速率差异的原因是______.
(3)废旧印刷电路板的回收利用可实现资源再生.经粉碎分离,能得到非金属粉末和金属粉末.用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,溶液变成蓝色,写出发生反应的化学方程式:______.
控制其它条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol/LH2SO4溶液处理,测得不同温度下铜的平均溶解速率(见下表)
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80
铜的平均溶解速率
(×10-3mol/(L?min))
7.34
8.01
9.25
7.98
7.24
6.73
5.76
|
当温度高于40℃时,铜的平均溶解速率随着反应温度的升高而下降,其主要原因是:______.
4、选择题 一定温度下,某密闭容器中发生反应:2HI(g) ?H2(g)+I2(g)?△H>0,若15s内c(HI)由0.1 mol・L-1降到0.07 mol・L-1,则下列说法正确的是
?H2(g)+I2(g)?△H>0,若15s内c(HI)由0.1 mol・L-1降到0.07 mol・L-1,则下列说法正确的是
A.15s内用H2表示的平均反应速率为v(H2)="0.002" mol・L-1・s-1
B.升高温度平衡逆向移动
C.c(HI)由0.07 mol・L-1降到0.05 mol・L-1所需时间为10s
D.减小反应体系的体积,化学反应速率加快
5、计算题 把2.5 mol A和2.5 molB两种气体混合放入容积为2L的密闭容器里发生反应3A(g)+B(g) XC(g)+2D(g),经5S后反应达到平衡,在此5S内C的平均反应速率为0.2mol/(L・ s),同时生成1 mol D,试求:
XC(g)+2D(g),经5S后反应达到平衡,在此5S内C的平均反应速率为0.2mol/(L・ s),同时生成1 mol D,试求:
⑴在此5S内D的平均反应速率。
⑵计算X的值