1��ѡ���� �����£�2.0��10-3mol?L-1������ˮ��Һ�У�������ҺpH��������Һ����仯���õ���[HF]��[F-]����ҺpH�ı仯��ϵ����ͼ��������������ȷ���ǣ�������
����ʾ��Ka��CH3COOH��=1.8��10-5mol?L-1��Ksp��CaF2��=1.5��10-10mol3?L-3��
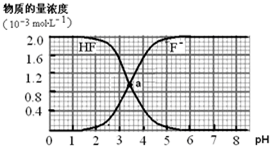
A���������߽���a��Ӧ��Һ��[F-]=[HF]
B������NaOH��Һ��pH=7����Һ��[F-]=[Na+]
C��������HF�ĵ��볣��Ka��HF����Ka��CH3COOH��
D��pH=4ʱ������CaCl2����ʹ[Ca2+]=2.0��10-3mol?L-1����CaF2��������
�ο��𰸣�A����������Ũ�ȣ���������ҺPH���������߽���a��Ӧ��Һ��[F-]=[HF]����A��ȷ��
B������NaOH��Һ��ӦHF+NaOH=NaF+H2O����Һ�д��ڵ���غ㣬c��Na+��+c��H+��=c��OH-��+c��F-������pH=7��c��H+��=c��OH-������Һ��[F-]=[Na+]����B��ȷ��
C��Ka=c(H+)c(F-)c(HF)����c��F-��=C��HF��ʱ��Ka=c��H+��=10-3.5=3.5��10-4mol?L-1��Ka��CH3COOH��=1.8��10-5mol?L-1��������HF�ĵ��볣��Ka��HF����Ka��CH3COOH������C��ȷ��
D������ͼ��PH=4.0����Һ�е�F-����Ũ��1.6��10-3mol������CaCl2����ʹc��Ca2+��=2.0��10-3mol?L-1��c��Ca2+����c2��F-��=2.0��10-3mol?L-1����1.6��10-3��2=5.1��10-10��Ksp��CaF2�����г������ɣ���D����
��ѡD��
���������
�����Ѷȣ���
2��ѡ���� ��֪ͬ�¶��µ��ܽ�ȣ�Zn��OH��2��ZnS��MgCO3��Mg��OH��2�����ܽ������S2-���������ԣ�FeS��H2S��CuS�����������ӷ���ʽ������ǣ�������
A��Mg2++2HCO3-+2Ca2++4OH-�TMg��OH��2��+2CaCO3��+2H2O
B��Cu2++H2S�TCuS��+2H+
C��Zn2++S2-+2H2O�TZn��OH��2��+H2S��
D��FeS+2H+�TFe2++H2S��
�ο��𰸣�A�������ܽ��MgCO3��Mg��OH��2����Ӧ����Mg��OH��2��CaCO3����A��ȷ��
B�����ڵ����S2-������H2S��CuS����Cu2+��H2S��Ӧ����CuS�����ӷ���ʽ��ȷ����B��ȷ��
C����ZnS��Zn��OH��2���ܣ�S2-��Zn2+Ӧ�Ƚ�ϳ�ZnS������������˫ˮ�⣬��C����
D�����ڵ����S2-������FeS��H2S��FeS�����������H2S����D��ȷ��
��ѡ��C��
���������
�����Ѷȣ���
3��ѡ���� ���л�ѧԭ����Ӧ�ã���Ҫ�ó����ܽ�ƽ��ԭ�������͵��ǣ�������
���ȴ�����Һ��ϴ����������ǿ��
������[BaCl2��Ba��NO3��2]����ʳ��ʳ��ʱ������0.5%��Na2SO4��Һ�ⶾ��
���ܶ���ɺ�����γɣ�
��̼�ᱵ�����������͡������ᱵ���ܣ�
����ĭ���������ԭ����
A���ڢۢ�
B���٢ڢ�
C���ۢܢ�
D���٢ڢۢܢ�
�ο��𰸣���̼������ǿ�������Σ���Ϊˮ��ʹ����Һ�ʼ��ԣ����ܴٽ���֬ˮ�⣬�����ȴ�����Һ��ϴ����������ǿ��Ӧ��������ˮ��ԭ�����ʲ����ϣ�
�ڱ������ж������Կ����Եı����ж��������Ӻ���������ӷ�Ӧ���ɲ��������ˮ�����ᱵ���������Ե��������������Ե�����ת�������Կ����ó����ܽ�ƽ��ԭ�������ͣ�
��ˮ�к��и����ӣ��������ж�����̼��������̼��ˮ��Ӧ����̼�ᣬ̼������ӷ�Ӧ���������Ե�̼��ƣ���ʱ�䷴Ӧ���γ��ܶ�ɺ�������Կ����ó���ƽ��ԭ�������ͣ�
��̼�ᱵ�ܺ����ᷴӦ�����Ȼ����Ͷ�����̼��ˮ�����ᱵ�������Ӧ������̼�ᱵ�����������͡������ᱵ���ܣ������ó���ƽ��ԭ�������ͣ�
��̼������ˮ��ʹ����Һ�ʼ��ԣ�������ˮ��ʹ����Һ�����ԣ������Ӻ����������ӷ�Ӧ����ˮ����̼�����ƺ���������ٽ�ˮ�⣬�Ӷ�Ѹ�ٵIJ���������̼�����Կ���������ˮ��ԭ����������ĭ���������ԭ�����ʲ����ϣ�
��ѡA��
���������
�����Ѷȣ���
4��ѡ���� �±��ṩ�IJ����������Dz���������ѡ��������������������Ӧʵ��Ŀ�ĵ���
ѡ��
| ʵ��Ŀ��
| ��������
| ʵ������
|
A
| ��п����ת��Ϊ��ͭ����
| �Թܡ���ͷ�ι�
| ��ɫ����ת��Ϊ��ɫ����
|
B
| ��֤CO2��������
| �ƾ��ơ�����ƿ������Ƭ
| þ������ȼ�գ�������ɫ��������ƿ�ڱ��а�ɫ��ĩ
|
C
| ������������������
| ��Һ©�����ձ�
| Һ��ֲ㣬�ϲ�Ϊ��ɫ��״Һ�壬�ϲ�Һ����²�Һ�嶼�ӷ�Һ©���¿ڷų�
|
D
| ʵ������ȡ��ϩ
| �ƾ��ơ�Բ����ƿ������
| ���Ⱥ�Һ����ڣ�Һ����ڣ������������
|
�ο��𰸣�A
���������A.ZnS��ɫ��������Һ�д��ڳ����ܽ�ƽ�⣺ZnS(s) Zn2+(aq)+S2-(aq)���������Һ�еμ�CuSO4��Һ������c(Cu2+)?c(S2-)>Ksp(CuS)�����Ի�ת��Ϊ�����ܵ�CuS��ɫ��������ȷ��B.þ����CO2�о���ȼ�գ�����ҫ�۵İ⣬�������̣������ǰ�ɫ������ƿ�ڱڸ��а�ɫ��ĩ�ͺ�ɫ����������C. ���������������ǻ��ܵ�Һ�����ʣ������������������м��뱥��̼������Һ�������á���Һ���ϲ����������Ӧ�ӷ�Һ©���Ͽڷų�������D.ʵ��������ϩ�轫Ũ�������Ҵ���ϼ���170�棬�����Ҫ�IJ���������ȱ���¶ȼƣ�����
Zn2+(aq)+S2-(aq)���������Һ�еμ�CuSO4��Һ������c(Cu2+)?c(S2-)>Ksp(CuS)�����Ի�ת��Ϊ�����ܵ�CuS��ɫ��������ȷ��B.þ����CO2�о���ȼ�գ�����ҫ�۵İ⣬�������̣������ǰ�ɫ������ƿ�ڱڸ��а�ɫ��ĩ�ͺ�ɫ����������C. ���������������ǻ��ܵ�Һ�����ʣ������������������м��뱥��̼������Һ�������á���Һ���ϲ����������Ӧ�ӷ�Һ©���Ͽڷų�������D.ʵ��������ϩ�轫Ũ�������Ҵ���ϼ���170�棬�����Ҫ�IJ���������ȱ���¶ȼƣ�����
���㣺����ʵ�鷽������Ƶ������жϵ�֪ʶ��
�����Ѷȣ�һ��
5������� ��12�֣�ˮ����һ����Ҫ�Ľ������ϣ�ˮ���ǿ��������ˮ����������Ҫָ�꣬����ˮ����CaO�ĺ����������õ�����ԣ��������������¿���ͨ���ⶨ����Ca0�ĺ���Ԥ��ˮ���ǿ�ȡ�Ϊ����ijƷ��ˮ���������Ƶĺ�������������ʵ�飺
����1��������ȷ��ȡ0��3000g�������������У���������5���Ӻ���ȴ�����飬����2��000g��ˮ̼���ƻ��Ⱥ��ٸ�������10���ӡ�
����2�����ܣ�ȡ��ȴ����ս�飬����40mLˮ���ټ���l0mLϡ�����3��ϡ���ᡣ
����3�����ӣ������ܺ�������Һ�������μ�ϡ��ˮʹ���е�Fe3+��Al3+ת��Ϊ���������ˡ�
����4������������Һ�м���������Һ��������к߽���ߵμӰ�ˮ�������ԣ����á�
����5���ܽ⣺�����ɵIJ���ƣ� CaC2O4���������뵽ϡ�����У����Ȳ�����ʹ����ȫ�ܽ⡣
����6���ζ�����0��1000 mol��L��1��KMnO4��Һ���еζ�����ɫ���ֲ�����30s����ʧ������ȥKMnO4��Һ13��000mL����Ӧ�Ļ�ѧ����ʽΪ��2 KMnO4+5 H2C2O4+3H2SO4= K2SO4+2MnSO4+5CO2��+8H2O
��1��д������3��Al3+ת��Ϊ���������ӷ���ʽ�� ��
��2����֪������Al��OH��3��Ksp=1��0��10��33����ʹ��Һ��c��Al3+����l��0xl0��6mol��L-1��pH�� ��
��3��ͨ������ȷ���������������Ƶ�����������д��������̣���
�ο��𰸣���1��Al3++3NH3?H2O=Al��OH��3��+3NH4+ (2) 5 (3) 60.7%
�����������1��ϡ��ˮ����Al3+��Ӧ������������������笠����ӣ�Al3++3NH3?H2O=Al��OH��3��+3NH4+����Ϊ��Al3++3NH3?H2O=Al��OH��3��+3NH4+��
��2����ʹ��Һ��c��Al3+����l��0��l0-6mol?L-1��C��OH-���� =
= =l��0��l0-9mol?L-1��
=l��0��l0-9mol?L-1��
c��H+����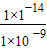 mol?L-1=l��0��l0-5mol?L-1������pH��5������5��
mol?L-1=l��0��l0-5mol?L-1������pH��5������5��
��3��5CaO�� 5CaC2O4 �� 2KMnO4
5��56g 2mol
m��CaO�� 0.1000mol?L-1��0.013L
 ��ã�m��CaO��=0.182g�������Ƶ���������Ϊ��
��ã�m��CaO��=0.182g�������Ƶ���������Ϊ�� ��100%=60.7%����Ϊ�������Ƶ���������Ϊ60.7%��
��100%=60.7%����Ϊ�������Ƶ���������Ϊ60.7%��
���㣺��������ܽ�ƽ��ļ��㣬���û�ѧ����ʽ�ļ����֪ʶ��
�����Ѷȣ�����