1、选择题 某MCFC型燃料电池可同时供应电和水蒸汽,其工作温度为600℃~700℃,所用燃料为氢气,电解质为熔融的K2CO3。该电池的总反应为:2H2+O2=2H2O,负极电极反应式为: H2+CO32――2e― H2O+CO2。则下列判断中正确的是 (? )?
H2O+CO2。则下列判断中正确的是 (? )?
A.放电时CO32―向负极移动
B.放电时CO32―向正极移动
C.正极反应: 4OH――4e―=2H2O+O2↑
D.当电池中生成1 mol水时,转移4 mol电子
参考答案:A
本题解析:根据题意知,该燃料电池燃料为氢气,电解质为熔融的K2CO3,总反应为2H2+O2=2H2O,负极反应为H2+CO32――2e― H2O+CO2,正极反应式:O2+2CO2+4e-
H2O+CO2,正极反应式:O2+2CO2+4e- 2CO32-。A、放电时CO32―向负极移动,正确;B、放电时CO32―应向负极移动,错误;C、正极反应式为:O2+2CO2+4e-
2CO32-。A、放电时CO32―向负极移动,正确;B、放电时CO32―应向负极移动,错误;C、正极反应式为:O2+2CO2+4e- 2CO32-,错误;D、当电池中生成1 mol水时,转移2 mol电子,错误。
2CO32-,错误;D、当电池中生成1 mol水时,转移2 mol电子,错误。
本题难度:一般
2、填空题 (17分)氢气和氨气都属于无碳清洁能。
(1)某些合金可用于储存氢,金属储氢的原理可表示为:M(s)+xH2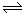 MH2x(s) △H<0(M表示某种合金)
MH2x(s) △H<0(M表示某种合金)
下图表示温度分别为T1、T2时,最大吸氢量与氢气压强的关系。则下列说法中,正确的是_____________
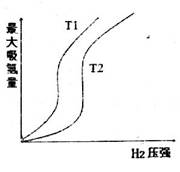
a.T1>T2
b.增大氢气压强,加快氢气的吸收速率
c.增大M的量,上述平衡向右移动
d.在恒温、恒容容器中,达平衡后充入H2,再次平衡后的压强增大
(2)以熔融碳酸盐为电解质,稀土金属材料为电极组成氢氧燃料电池(如装置甲所示),其中负极通入H2,正极通入O2和CO2的混合气体。乙装置中a、b为石墨电极,电解过程中,b极质量增加。
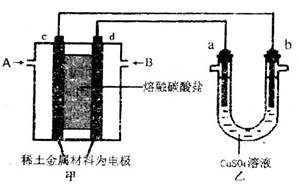
①工作过程中,甲装置中d电极上的电极反应式为_____________________________。
②若用该装置电解精炼铜,则b极接____(填“粗铜”或“精铜”);若用该装置给铁制品上镀铜,则____(填“a”或“b”)极可用惰性电极(如Pt电极),若电镀量较大,需要经常补充或更换的是_______。
(3)氨在氧气中燃烧,生成水和一种空气组成成分的单质。
已知:N2(g)十3H2(g) 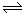 2NH3(g) △H=
2NH3(g) △H=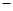 92.4kJ・mol-1
92.4kJ・mol-1
2H2(g)十O2(g)=2H2O(1) △H=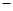 572KJ・mo1-1
572KJ・mo1-1
试写出氨气在氧气中燃烧生成液态水的热化学方程式___________________。
(4)在一定条件下,将lmotN2和3molH2混台于一个10L的密闭容器中发生反应:
N2(g)十3H2(g) 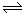 2NH3(g)
2NH3(g)
5min后达到平衡,平衡时氮气的转化率为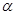 。
。
①该反应的平衡常数K=________,(用含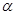 的代数式表示)
的代数式表示)
②从反应开始到平衡时N2的消耗速率v(N2)=____mo1・L-1・min-1。(用含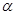 的代数式表示)
的代数式表示)
参考答案:本题共17分
(1)b(2分)
(2)①O2+4e-+2CO2=2CO32-(2分)
②精铜(2分) a(2分) CuSO4溶液(2分)
(3)4NH3(g)+ 3O2(g)=2N2(g)+6H2O(l) △H=-1531.2kJ・mol-1(3分)
或2NH3(g)+ 3/2O2(g)=N2(g)+3H2O(l) △H=-765.6.kJ・mol-1
(4)①400α2/27(1-α)4(2分)
②0.02α(2分)
本题解析:(1)a、温度升高,平衡逆向移动,则吸氢量减少,所以T1<T2,错误;b、增大氢气压强,则增大反应速率,加快氢气的吸收速率,正确;c、M是固体,所以增大M的量,上述平衡不移动,错误;d、在恒温、恒容容器中,达平衡后充入H2,压强增大,平衡正向移动,再次平衡后的压强减小,错误,答案选b;
(2)①甲为原电池,则乙为电解池,反应中b极质量增加,说明b极是阴极,有Cu析出,所以c是原电池负极,d是原电池正极,a是电解池阳极;d极为氧气、二氧化碳发生还原反应,得到电子生成碳酸根离子,电极反应式为O2+4e-+2CO2=2CO32-;
②若用该装置电解精炼铜,则粗铜做阳极,精铜作阴极,b极是阴极,所以b极是精铜;若用该装置给铁制品上镀铜,则铜作阳极,铁作阴极,所以b极一定是铁制品,则a极可用惰性电极;因为铜离子放电析出,需经常补充或更换的是CuSO4溶液;
(3)根据盖斯定律,将所给两个热化学方程式中的氢气消去,可得氨气与氧气反应的热化学方程式,得4NH3(g)+ 3O2(g)=2N2(g)+6H2O(l) △H=-1531.2kJ・mol-1;
(4)① N2(g)十3H2(g) 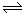 2NH3(g)
2NH3(g)
开始(mol/L) 0.1 0.3
转化(mol/L) 0.1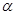 0.3
0.3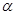 0.2
0.2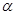
平衡(mol/L)0.1(1-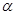 ) 0.3(1-
) 0.3(1-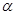 ) 0.2
) 0.2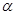
所以该反应的平衡常数K=(0.2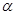 )2/[0.1(1-
)2/[0.1(1-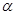 )] ・[ 0.3(1-
)] ・[ 0.3(1-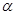 )]3=400α2/27(1-α)4;
)]3=400α2/27(1-α)4;
②从反应开始到平衡时N2的消耗速率v(N2)=0.1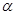 /5min=0.02α.
/5min=0.02α.
考点:考查条件对平衡的影响,平衡常数、反应速率的计算,电化学反应原理的应用,
本题难度:困难
3、选择题 热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是
A.正极反应式:Ca + 2Cl--2e- = CaCl2
B.放电过程中,Li+向负极移动
C.每转移0.1mol电子,理论上生成20.7 g Pb
D.常温时,在正负极间接上电流表或检流计,指针不偏转
参考答案:D
本题解析:A、正极发生还原反应,故为PbSO4+2e-=Pb+SO42-,错误;B、放电过程为原电池,阳离子向正极移动,错误;C、每转移0.1mol电子,生成0.05mol Pb,为10.35g,错误;D、常温下,电解质不能融化,不能形成原电池,故指针不偏转,正确。
【考点定位】考查电化学基本理论,涉及电极判断、电极反应方程式的书写、离子流动方向以及简单计算。
本题难度:简单
4、选择题 锂钒氧化物电池的能量密度远远超过其它材料电池,其成本低,便于大量推广,且对环境无污染。电池总反应式为:V2O5+xLi==LixV2O5。下列说法中,不正确的是
[? ]
A.正极材料为锂,负极材料为V2O5
B.向外供电时,锂离子在凝胶中向正极移动
C.正极的电极反应式为:V2O5 + xLi++ xe-== LixV2O5
D.负极的电极反应式为:xLi-xe-==xLi+
参考答案:A
本题解析:
本题难度:一般
5、选择题 如下图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)
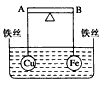
[? ]
A.杠杆为导体和绝缘体时,均为A端高B端低
B.杠杆为导体和绝缘体时,均为A端低B端高
C.当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低
D.当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高
参考答案:D
本题解析:
本题难度:一般