1��ѡ���� �������͵ķ�Ӧ�У�һ������������ԭ��Ӧ����
A�����Ϸ�Ӧ
B���û���Ӧ����
C���ֽⷴӦ
D�����ֽⷴӦ
�ο��𰸣�B
���������������ԭ��Ӧ��һ���л��ϼ۵ĸı䣬��������Ӧ�����е��û���Ӧ���ض���ͬ��Ԫ���ڻ���̬������̬֮���ת�������ϼ�һ������������ѡ��B��������
�����Ѷȣ�һ��
2��ѡ���� ������ʵ�������������ʵ�ֵķ�Ӧ�ǣ�?��
A PCl5 PCl3? B. MnO2
PCl3? B. MnO2 Mn2+
Mn2+
C.SO2 SO32-? D. Fe
SO32-? D. Fe Fe3O4
Fe3O4
�ο��𰸣�D
������������������������ԣ�������ԭ��Ӧ�����ϼ۽��ͣ���ԭ�����л�ԭ�ԣ�����������Ӧ�����ϼ����ߡ��ʼ�����������Ӧ��Ԫ�ػ��ϼ����ߡ��ݴ˴��⡣
A����Ԫ�ػ��ϼ۽��ͣ�������ԭ��Ӧ��Ӧ���뻹ԭ����
B����Ԫ�ػ��ϼ۽��ͣ�������ԭ��Ӧ��Ӧ���뻹ԭ����
C����Ԫ�ػ��ϼ�û�з����仯��û�з���������ԭ��Ӧ�������������������ԭ����
D����Ԫ�ػ��ϼ����ߣ�����������Ӧ�����������������
��ѡD
�����Ѷȣ���
3������� ��6�֣���˫���ŷ�������з�Ӧ�е���ת�Ƶķ������Ŀ��
MnO2 + 4HCl��Ũ��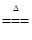 ?Cl2�� + MnCl2 + 2H2O
?Cl2�� + MnCl2 + 2H2O
���У���������?��?Ԫ�ر�������
�ο��𰸣���6�֣�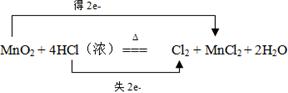 ?MnO2��Cl
?MnO2��Cl
������������ݷ���ʽ��֪����Ԫ�صĻ��ϼ۴ӣ�1�����ߵ�0��ʧȥ1�����ӣ������Ԫ�ر���������Ԫ�صĻ��ϼ۴ӣ�4�۽��͵���2�ۣ��õ�2�����ӣ����Զ�����������������
����������ʧȥ���ӣ�����Ԫ�ػ��ϼ����ߵ�����ԭ������֮�õ����ӣ���������Ԫ�ػ��ϼ۽��͵������������ݴ˿��Խ����й��жϡ������ʾ������ԭ��Ӧ�ķ����������ǵ����ţ�ע�����ֶ��ߡ�
�����Ѷȣ�һ��
4������� ��1L1.0mol?L-1NaOH��Һ����17.92LCO2����״��������Һ������䣮��������Һ�е�CO32-��HCO3-�����ʵ���Ũ�ȣ�
����֪���ܵķ�ӦΪ��2NaOH+CO2�TNa2CO3+H2O��Na2CO3+H2O+CO2�T2NaHCO3��
�ο��𰸣�1L1.0mol/LNaOH��Һ���������Ƶ����ʵ���Ϊ1L��1.0mol/L=1mol��
17.92LCO2����״���������ʵ���Ϊ17.92L22.4L/mol=0.8mol��
����Һ��Na2CO3��NaHCO3�����ʵ����ֱ�Ϊxmol��ymol�����������ӡ�̼ԭ���غ��з��̣���
���������
�����Ѷȣ�һ��
5��ѡ���� ��������������һ���漰��ѧ�仯����
A����ɫ��Ӧ
B�������ЧӦ
C��ʯ�͵ķ���
D���������Һ����
�ο��𰸣�D
���������A����ɫ��Ӧ���������仯��B�������ЧӦ�������仯��C��ʯ�ͷ����������仯��D���������Һ���緢���缫��Ӧ�����ڻ�ѧ�仯��ѡD��
�����Ѷȣ���