1、选择题 有关电解质的说法正确的是( )
A.NaOH固体溶于水后能导电,所以NaOH是电解质
B.CO2水溶液的能够导电,所以CO2是电解质
C.液态的铜导电性很好,所以铜是电解质
D.FeCl3溶液能够导电,所以FeCl3溶液是电解质
参考答案:A
本题解析:
本题难度:一般
2、选择题 根据酸碱质子理论,凡是能给出质子的分子或离子都是酸,凡是能结合质子的分子或离子都是碱。按照这个理论,下列微粒属于两性物质的是:
①HS-②CO32-③H2PO4-④NH3⑤H2S⑥CH3COOH⑦OH-⑧H2O⑨NO2- ⑩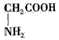
[? ]
A.①⑤
B.③⑥
C.①②⑨
D.①③⑧⑩
参考答案:D
本题解析:
本题难度:一般
3、选择题 叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是( )
A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3?)>c(OH?)
B.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3?)>c(OH?)>c(H+)
C.HN3与NH3作用生成的产物是共价化合物
D.N3-与CO2含相等电子数
参考答案:C
本题解析:
本题难度:简单
4、简答题 室温下有①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液各25mL,下列说法正确的是( )
A.物质的量浓度均为0.1mol/L,3种溶液pH的大小顺序是③>②>①
B.物质的量浓度均为0.1mol/L,将3种溶液稀释相同倍数,pH变化最大的是②
C.物质的量浓度均为0.1mol/L,分别加入25mL0.1mol/L盐酸后,pH最大的是①
D.pH均为9时,3种溶液的物质的量浓度的大小顺序是②>③>①
参考答案:A.等浓度时强碱的pH最大,强碱弱酸盐中对应的酸性越强,水解程度越小,碳酸的酸性小于醋酸的,所以三种溶液pH的大小顺序是③>①>②,故A错误;
B.稀释时强碱的变化程度大,所以三种溶液稀释相同倍数,pH变化最大的是③,故B错误;
C.等体积等浓度混合后,①中溶质为NaHCO3、NaCl,②中溶质为NaCl、CH3COOH,③中溶质为NaCl,HCO3-离子水解显碱性,所以pH最大的是①,故C正确;
D.三种溶液的pH均为9,c(OH-)=10-5mol/L,c(NaOH)=10-5mol/L,但碳酸的酸性小于醋酸的酸性,所以c(Na2CO3)>c(CH3COONa)>10-5mol/L,所以三种溶液的pH均为9,则物质的量浓度的大小顺序是①>②>③,故D错误;
故选C.
本题解析:
本题难度:一般
5、选择题 下列电离方程式,书写正确的是
A.Al2(SO4)3 =2Al3+ + 3SO42-
B.Na2CO3= Na++ CO32?
C.Mg(NO3)2 = Mg+2 +2NO3-
D.KMnO4 =K+ +Mn7+ +4O2-
参考答案:A
本题解析:略
本题难度:简单