1、选择题 几位同学在一起讨论问题,你认为正确的是(?)
A.水溶液中有离子参加的反应就是离子反应
B.离子反应是指在水溶液中进行的反应
C.参加离子反应的物质必须都是电解质
D.凡是没有沉淀、气体和水生成的反应都不是离子反应
参考答案:A
本题解析:有离子参加的反应就是离子反应,并不一定在水溶液进行,故A项正确,B项错误;参加离子反应的物质不一定都是电解质,如单质与离子的反应,也是离子反应,故C项错误;有沉淀、气体和水生成的反应只是复分解反应这一类离子反应的条件,对于单质与离子间的置换反应类的反应就不符合,故D项错误。
本题难度:简单
2、选择题&n bsp; 根据下表提供的数据,判断在等浓度的NaCN和NaHS的混合溶液中,各种离子浓度关系正确的是
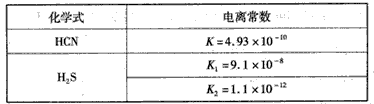
[? ]
A.c(CN -)>c(HS -)>c(OH -)
B.c(HS -)>c(CN -)>c(OH -)
C.c(Na+)+c(H+)=c(HS -)+c(CN-)+c(OH -)
D.c( HCN) +c(CN -)=c(HS -)+c( H2S)
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列有关NaHCO3与NaHSO4的比较叙述正确的是
A.两者在水溶液中电离方程式相似
B.两者在熔融状态电离方程式相似
C.两者都是酸
D.两者都是强电解质
参考答案:D
本题解析:A? NaHCO3=Na++HCO3-;NaHSO4=Na++H++SO42-。B在熔融状态下NaHCO3分解生成碳酸钠,二氧化碳和水。NaHSO4=Na++HSO4-C两者都属于酸式盐,D在水溶液中能完全电离的电解质是强电解质,所以D正确
本题难度:一般
4、填空题 (6分)下列物质:①铜丝②碳酸③氯化氢气体④稀硝酸⑤二氧化硫气体⑥氨水⑦蔗糖晶体⑧熔融氯化钠⑨氧化钠固体⑩硫酸铜晶体(用相应序号填空)
⑴上述物质可导电的是_________________⑵属于电解质的是__________________
(3)属于强电解质的是?
参考答案:(每空2分,共6分)? (1)①④⑥⑧? (2)②③⑧⑨⑩? (3)③⑧⑨⑩
本题解析:(1)电解质只有溶于水或在熔融状态下才能导电,所以可以导电的是①④⑥⑧。
(2)溶于水或在熔融状态下,能够自身电离出阴阳离子的化合物是电解质,所以属于电解质的是②③⑧⑨⑩。
(3)在溶液中完全电离出阴阳离子的电解质是强电解质,属于属于强电解质的是③⑧⑨⑩。
本题难度:一般
5、选择题 下列电离方程式中,正确的是(?)
A.CH3COOH = CH3COO- + H+
B.KClO3 K+ + ClO3-
K+ + ClO3-
C.NaOH = Na+ + OH-
D.NaHSO4 = Na+ +HSO4-
参考答案:C
本题解析:A不正确,醋酸是弱酸,应该用可逆号连接;B不正确,氯酸钾是强电解质,用等号连接;D不正确,应该是NaHSO4 = Na++ H+ +SO42-,答案选C。
点评:用化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水时电离成离子的化学方程式。书写电离方程式时应特别注意:
①写出物质正确的化学式是正确书写电离方程式的基础。
②要正确书写出电离的阳离子、阴离子的符号。这里注意区分离子符号和化合价的书写。离子所带电荷的数目应标在元素符号的右上角,且要先写数字,后写“+”或“-”号;化合价标在元素符号的正上方,先写“+”或“-”号,后写数字。离子的电荷数为1时,1省略不写,只写“+”或“-”号;而化合价数为1时,1必须标明。
③含有原子团的物质电离时,原子团应作为一个整体,不能分开。
④表示离子数目的数字要写在离子符号的前面,不能像在化学式里那样写在右下角。
⑤在电离方程式中,阴阳离子所带正负电荷的总数必须相等。
⑥酸碱盐电离出的阴、阳离子的个数应与其化学式中相应原子或原子团的个数相同,电离出的离子所带的电荷数应与该元素或原子团的化合价数值相等。
⑦强电解质用等号,弱电解质一律用可逆号,多元弱酸分步电离,多元弱碱一步电离。强酸的酸式盐一步电离。弱酸的酸式盐分步电离,第一步不可逆,以后步步可逆,且一步比一步的电离程度小。
本题难度:简单