1������� �±��г���A��M 13��Ԫ�������ڱ��е�λ�ã�
1
| A
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
2
| ?
| ?
| ?
| B
| C
| D
| E
| ?
|
3
| F
| G
| H
| ?
| ?
| I
| J
| K
|
4
| L
| M
| ?
| ?
| ?
| ?
| ?
| ?
|
��1����ЩԪ���У���������ǿ��Ԫ����_______����Ԫ�����ƣ��� ͬ�����ǽ�������ǿ����__________������õ�Ԫ��
ͬ�����ǽ�������ǿ����__________������õ�Ԫ�� ��_________��
��_________��
��2��д��HԪ�ص�����������Ӧ��ˮ����ֱ���FԪ�ص�����������Ӧ��ˮ���JԪ���⻯���ˮ��Һ��Ӧ�����ӷ���ʽ_________?________��?��
��3��I2����J����L����M2�������У��뾶������________����С����__________��
��4��A��D�γɵĻ�����A2D2��___________����������ʽΪ_____________________��
�ο��𰸣�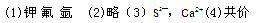
�����������
�����Ѷȣ���
2��ѡ���� ��֪ij���ᡢ����ͭ���������Ļ��Һ100mL�У����������ӵ����ʵ���Ũ����ȣ���������ӵ�Ũ��Ϊ6mol?L-1�������Һ�п��ܽ����۵�����Ϊ��������
A��5.6g
B��11.2g
C��16.8g
D��22.4g
�ο��𰸣�n��SO42-��=0.1L��6mol/L=0.6mol��
��Һ�и��������ӵ����ʵ�����ȣ��������ӵ����ʵ����ֱ�Ϊxmol�����ݵ���غ�ɵã�
x+2x+3x=2��0.6��
���x=0.2����
2H++Fe=Fe2++H2��
0.2 0.1
Cu2++Fe=Fe2++Cu
0.2 0.2
2Fe3++Fe=Fe2+��
0.2 0.1
������0.1+0.2+0.1=0.4molFe��
������Ϊ0.4mol��56g/mol=22.4g��
��ѡD��
���������
�����Ѷȣ�һ��
3������� I����Ҫ�������пո�����������л�����й�ʽ�ӣ�
��Է���������С���л������ʽ______��ʳ���е��л���ṹʽ______����������Һ�к�������ṹ��ʽ______��
II���������﮺�þ����Ԫ�����ڱ��о�������ġ��Խ��߹�ϵ�������ʼ������������ʮ�����ƣ��밴Ҫ��ش����и��ʣ�
��1��д��Be��NaOH��Һ��Ӧ�����ӷ���ʽ������Na2BeO2����______��
��2��Be��OH��2��Mg��OH��2�����Լ�______���������ӷ���ʽΪ��______��
�ο��𰸣�I����̼���������4�����ӣ��������1�����ӣ�һ��̼�γ�4�Թ��õ��Ӷԣ�һ���γ�һ�Թ��õ��Ӷԣ����Ե���ʽΪ��

��?
��̼Ҫ�γ�4��������Ҫ�γ�2��������Ҫ�γ�1��������������ĽṹʽΪ

��?
����������Һ�к��������������ǣ�����������һ�����ǻ�ȩ��6��̼ԭ����ͬһ�����ϣ����������ǵĽṹ��ʽΪ��CH2OH-CHOH-CHOH-CHOH-CHOH-CHO��
�ʴ�Ϊ��

��

��CH2OH-CHOH-CHOH-CHOH-CHOH-CHO��?
II����1��������NaOH��Һ��Ӧ����ƫ�����ƺ������������������ʮ�����ƣ�����Be+2NaOH�TNa2BeO2+H2�����ʴ�Ϊ��Be+2OH-�TBeO22-+H2����
��2�����������������ԣ�Be��OH��2Ҳ�����ԣ�����Be��OH��2��Mg��OH��2�����Լ�NaOH��Һ���𣬻�ѧ����ʽΪBe��OH��2+2NaOH�TNa2BeO2+2H2O��
�ʴ�Ϊ��NaOH��Һ��Be��OH��2+2OH-�TBeO22-+2H2O��
���������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�������
A���ƺ���ˮ��ӦNa+2H2O=Na++2OH-+H2��
B������Ͷ�뵽NaOH��Һ�У�2Al+2OH-�T�T2AlO2-+H2��
C��AlCl3��Һ�м��������İ�ˮ��Al3++3OH-�T�TAl��OH��3��
D��FeCl2��Һ��Cl2��Ӧ��2Fe2++Cl2=2Fe3++2Cl-
�ο��𰸣�A���ƺ���ˮ��Ӧ��ʵ���ǣ�2Na+2H2O=2Na++2OH-+H2�������ӷ�ӦҪ��ѭ����غ㣬��A����
B�����ܺ�ǿ�Ӧ����ƫ�����κ�������ʵ���ǣ�2H2O+2Al+2OH-�T�T2AlO2-+3H2������B����
C����ˮ����������ӷ���ʽ�в��ܲ�����ӵ���ʽ��AlCl3��Һ�м��������İ�ˮ�ķ�ӦΪ��Al3++3NH3?H2O�T�TAl��OH��3��+3NH4++3H2O����C����
D�������ܼ�������������Ϊ����������2Fe2++Cl2=2Fe3++2Cl-����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ��ȷ���ǣ�?��
A����ʯī���缫����Ȼ�����Һ��2Cl��+2H2O= 2OH��+H2��+Cl2��
B��FeBr2��Һ��ͨ������������2Fe2++2Br-+2Cl2 = 2Fe3++Br2+4Cl-
C��Fe3O4��HCl��Fe3O4+8H+=2Fe3++Fe2++4H2O
D��Fe2O3��HI��Fe2O3+6H+=2Fe3++3H2O
�ο��𰸣�C
���������A����Һ�е��������������ɵ�OH�����ܹ��棻B��Ҫ��������������FeBr2��ȫ��������2Fe2++4Br-+3Cl2 = 2Fe3++2Br2+6Cl-��D��Fe3+��I��������������ԭ��Ӧ���ʴ�ΪC
�����Ѷȣ�һ��