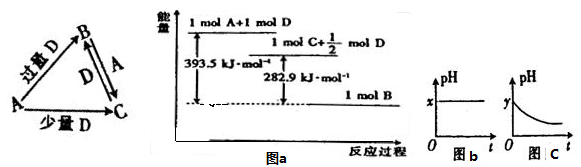
1������� A��B��C��D��Ϊ��ѧ��ѧ�г����ĵ��ʻ������֮��Ĺ�ϵ��ͼ��ʾ�����ֲ�������ȥ����
 ?
?
��1����AΪ�������ʣ�D��ijǿ���ϡ��Һ����ӦC+D��B�����ӷ���ʽΪ?��
��2����A��BΪ�Σ�DΪǿ�A��ˮ��Һ�����ԣ���
��C�Ļ�ѧʽΪ?��
�ڷ�ӦB+A��C�����ӷ���ʽΪ?��
��3����AΪǿ�DΪ��̬���������ʱ����B��ˮ��Һ¶���ڿ����У���pH��ʱ��t�仯��������ͼ��ͼb��ͼc��ʾ��������D���ܽ��ˮ�Ļӷ�����
����ͼb������ʵ����D�Ļ�ѧʽΪ?��
����ͼc������ʵ,����pH�仯��ԭ����?�������ӷ���ʽ��ʾ����
��4����AΪ�ǽ������ʣ�D�ǿ�������Ҫ�ɷ�֮һ������֮��ת��ʱ�����仯����ͼa����д��A+D��C���Ȼ�ѧ����ʽ?��
�ο��𰸣���1��3Fe2++NO3-+4H+=3Fe3++NO��+2H2O
��2����Al(OH)3
��Al3++3AlO2-+6H2O=4Al(OH)3��
��3����CO2 ��2HSO3-+O2=2H++2SO42-
��4��C(s)+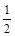 O2(g)="CO(g)" �SH=-110.6kJ/mol
O2(g)="CO(g)" �SH=-110.6kJ/mol
�����������1��AΪ�������ʣ���D���ϡ��Һ�����IJ�ͬ�����ﲻͬ����A�DZ�۽���������Fe��D����������ԣ�ϡ��Һ���������Ե�����HNO3����C+D��B��ӦΪ3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
��2��A��BΪ�Σ�A��ǿ��D��Һ�����IJ�ͬ�����ﲻͬ��A��ˮ��Һ�����ԣ�����Al3+��CΪAl(OH)3��B+A��CΪAl3++3AlO2-+6H2O=4Al(OH)3����
��3��AΪǿ�DΪ��̬�����DΪ��Ԫ��������������CO2��SO2��bͼ��pH���䣬ΪCO2��pH��С����SO2����Ϊ�������ڿ�����������Ϊ����ʹpH��С����2HSO3-+O2=2H++2SO42-��
��4��AΪ�ǽ������ʣ�������Ҫ�ɷ�D��Ӧ��O2��������ϵ������Ӧ������A+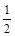 O2��C��C+
O2��C��C+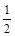 O2��B��AԪ����+2��+4�ۣ���A��̼��A+D��C���Ȼ�ѧ����ʽ��C(s)+
O2��B��AԪ����+2��+4�ۣ���A��̼��A+D��C���Ȼ�ѧ����ʽ��C(s)+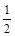 O2(g)="CO(g)" �SH=-110.6kJ/mol��
O2(g)="CO(g)" �SH=-110.6kJ/mol��
�����Ѷȣ�һ��
2��ѡ���� ����������ȷ����
A��Fe��������ȼ������FeCl2
B����AlCl3��Һ��ε��뵽NaOH��Һ���Ȳ�����ɫ��������������ʧ
C�������л������ۼȿ��ù�����NaOH��Һ��Ҳ�����ù���FeCl3��ַ�Ӧ���˳�ȥ
D�������£�����Ʒ��Ũ�����Ũ���ᴦ����������ʴ
�ο��𰸣�D
���������A.? Fe��������ȼ������FeCl3;���� B?��AlCl3��Һ��ε��뵽NaOH��Һ����ʼ���������ɫ����������C�������л������ۼȿ��ù�����NaOH��Һ���������ù���FeCl3��ַ�Ӧ����ΪFe��FeCl3Ҳ��Ӧ������D��ȷ��
�����Ѷȣ�һ��
3��ѡ���� ��100 mL 3 mol��L-1 NaOH��Һ��100 mL 1 mol��L-1 AlCl3��Һ�����������ַ�������ʵ�飺�ٽ�����������Һ�ֶ�μӵ�AlCl3��Һ�У��ڽ�AlCl3��Һ�ֶ�μӵ�NaOH��Һ�С��Ƚ�����ʵ��Ľ����
A��������ͬ�����������
B������ͬ������������
C��������ͬ������������
D������ͬ�����������
�ο��𰸣�D
���������������Ϊ�ȳ���������ܽ⣻������Ϊ���������г������ɡ���Ӧ�������������ˣ��ʳ���������ȵġ���ѡD��
���������⿼���������Ӧ��֪ʶ�ͻ�ѧ���㣬AlCl3��Һ�ֺ�NaOH�ܷ�Ӧ����������μ�˳��ͬ��Ӧ�Ͳ�ͬ��ԭ���ǽ���Ĺؼ�����Ŀ�Ѷ����С�
�����Ѷȣ�һ��
4��ѡ���� �� MgCl2��Al2(SO4)3�Ļ����Һ�������в��ϼ���NaOH��Һ���õ��ij�����������NaOH��Һ�Ĺ�ϵ��ͼ��ʾ����ԭ��Һ��MgCl2��Al2(SO4)3�����ʵ���Ũ��֮��Ϊ
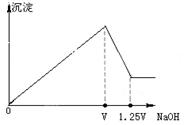
A��1��1
B��2��1
C��3��2
D��2��3
�ο��𰸣�A
�����������MgCl2��Al2(SO4)3�Ļ����Һ��μ���NaOH��Һ��������ӦMg2++2OH-= Mg(OH)2��, Al3++3OH-=Al(OH)3��.���Գ��������ࡣ��NaOH����ʱ�з�����Ӧ��Al(OH)3+OH-=AlO2-+2 H2O.��������С��������������ȫ�ܽ������ﵽ��Сֵ�������ڳ����ܽ�ķ�Ӧ��n(Al(OH)3):n(OH-) =1:1,n(OH-)=0.25V,����n(Al3+)=n(Al(OH)3)= n(OH-)=0.25V,n(Al2(SO4)3)=1/2n(Al3+)=0.125V.ʹAl3+�����������ĵ����������ӵ����ʵ���Ϊ3n(Al3+)=0.75V,������ӦMg2++2OH-= Mg(OH)2��,���ĵ����������ӵ����ʵ���ΪV-0.75V=0.25V�����MgCl2�����ʵ���Ϊ1/2n(OH-)=0.125V.����ԭ��Һ��MgCl2��Al2(SO4)3�����ʵ���֮��Ϊ0.125V��0.125V=1:1.���ѡ��ΪA��2��Al2(SO4)3�Ļ����Һ��NaOH��Һ������Ӧ�������֪ʶ��
�����Ѷȣ�һ��
5��ѡ���� ���м��ֽ�����Ʒ�ĶƲ�������ʴ������������(����)
A��������Ͱ
B��ʳƷ����ͷ��(����)
C������ˮͰ(��п)
D������ͭ�ʽ���
�ο��𰸣�B
����������ؼ��ǿ����Ʋ���¶���Ľ�����Ʋ��ܷ��γ�ԭ��أ��γ�ԭ��ؽ����Ƿ��Ǹ�����������Ͱ�Ʋ������������������ʴ��ʳƷ����ͷ��(����) �Ʋ������������������ʴ������ˮͰ(��п) �Ʋ������п����������ʴ������ͭ�ʽ��¶Ʋ������ͭ����������ʴ�����������Ļ�����ǿ��ͭ�ģ�����ѡ��B��ȷ��
�����Ѷȣ���