1、选择题 物质的量为0.20 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为
A.6.4g
B.8.0g
C.8.4g
D.9.2g
参考答案:D
本题解析:若气体只有CO2,有2Mg+CO==2MgO+C可知,0.20 molMg生成0.20 molMgO和0.10molC,共计9.2g,因含有O2而低于此计量,但多余Mg自身质量4.8g。故选D。
本题难度:一般
2、填空题 锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为_______________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式 ____________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是____________________。(填序号)
① 硫酸铝和氢氧化钠 ② 硫酸铝和氨水③ 硫酸锌和氢氧化钠④ 硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式 __________________________。试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因_______________________
参考答案:(1)AlO2-(或Al(OH)4-)
(2)Zn+2NaOH==Na2ZnO2+H2↑ (或Zn+2NaOH+2H2O==Na2Zn(OH)4+H2↑)
(3)①③④
(4)Al3++3NH3・H2O==Al(OH)3↓+3NH4+;可溶性锌盐与氨水反应产生的Zn(OH)2可溶于过量氨水中,生成Zn(NH3)42+,氨水的用量不易控制
本题解析:
本题难度:一般
3、选择题 在实际生活中,下列说法正确的是( )
A.糖尿病是食用食糖过量造成的
B.日常生活中常用无水乙醇杀菌消毒
C.绿色食品是不含任何化学物质的食品
D.家庭中不宜长期食用铝质餐具盛放菜、汤等食物
参考答案:A.胰岛分泌的激素是对人体有特殊作用的物质,能调节的糖的代谢,胰岛素分泌不足易患糖尿病,故A错误;
B.在75%的酒精作用下,乙醇能渗入细胞内,使蛋白质凝固变性,从而起到杀菌的作用,低于这个浓度,其渗透脱水作用减弱,杀菌力不强;而高于此浓度,则会使细菌表面蛋白质迅速脱水,凝固成膜,妨碍乙醇透入,削弱杀菌能力,对病毒无效,故B错误;
C.绿色食品是指在无污染的条件下种植、养殖、施有机肥料、不用高毒性、高残留农药、在标准环境、生产技术、卫生标准下加工生产、经权威机构认定并使用专门标志的安全、优质、营养类食品的统称,任何物质都由化学物质组成,故C错误;
D.铝锅放置在空气中被氧化为氧化铝,氧化铝具有两性,既能与酸反应又能与碱反应,生成物易溶于水,内层的铝,不宜长期盛放酸性或碱性食物,因为金属铝能与它们发生反应,铝与氢氧化钠溶液反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑生成偏铝酸钠易溶于水,所以家庭中不宜长期食用铝质餐具盛放菜、汤等食物,故D正确;
故选D.
本题解析:
本题难度:简单
4、填空题 Al及其化合物在工业上有极其广泛的用途,
(1)焊接钢轨时用Al冶炼Fe的反应方程式为?;铝的化合物明矾可用于净水,其原理用离子方程式解释为?。
(2)硅藻遗骸中主要成分是Al2O3、SiO2和Fe2O3。从中获取Al(OH)3的过程如下:
步骤I:取适量硅藻遗骸用70%H2SO4浸泡;
步骤II:向上述浸泡液中加入过量NaOH并过滤;
步骤III:向上述滤液中通入过量CO2过滤得到Al(OH)3。
①用70%H2SO4浸取硅藻遗骸的目的是?。
②步骤II中涉及铝元素的离子方程式为?;
③步骤III中能否用HCl代替CO2??(填“能”或“不能”);该步骤所得滤液中存在的电荷守恒式为?;向该滤液中滴加少量NaOH溶液,则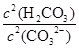 ?填(“变大”、“变小”或“不变”)
?填(“变大”、“变小”或“不变”)
(3)Al(OH)3可用作阻热材料,试从Al(OH)3的化学性质角度分析其原因?。
参考答案:
(1)Fe2O3+2Al Al2O3+2Fe(2分)? Al3++3H2O=Al(OH)3(胶体)+3H+(2分)
Al2O3+2Fe(2分)? Al3++3H2O=Al(OH)3(胶体)+3H+(2分)
(2)①从硅藻遗骸中浸取出Al3+和Fel3+(1分)
②Al3++4OH-=AlO2-+2H2O(或Al3++3OH-=Al(OH)3↓? Al(OH)3+OH-=AlO2-+2H2O)( 2分)
③不能(1分) c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+2c(SO42-)(2分)?变小(1分)
(3)Al(OH)3的分解反应为吸热反应
本题解析:本题是通过工业上Al及其化合物在工业上的用途以及Al(OH)3的分离与制备。
(1)一个是铝热反应的用途―焊接钢轨或者用来冶炼金属,可溶性铝盐净水,主要是利用Al3+的水解
得到Al(OH)3(胶体)吸附悬浮物达到净水的目的。Fe2O3+2Al Al2O3+2Fe,Al3++3H2O=Al(OH)3(胶体)+3H+。这两个方程式注意条件,前面是高温,后面需注意用“=”号并且要写 “胶体”二字。
Al2O3+2Fe,Al3++3H2O=Al(OH)3(胶体)+3H+。这两个方程式注意条件,前面是高温,后面需注意用“=”号并且要写 “胶体”二字。
(2) 通过从Al2O3、SiO2和Fe2O3中获取Al(OH)3:用H2SO4浸泡溶解Al2O3和Fe2O3,剩余SiO2,然后进行过滤得到固体(SiO2)和滤液(Al3+和Fel3+,SO42-等)。然后向上述浸泡液中加入过量NaOH后得到Fe(OH)3↓和NaAlO2和NaOH的混合溶液并进行过滤。在往上述滤液中通入过量CO2过滤得到Al(OH)3↓和NaHCO3溶液。
①用70%H2SO4浸取硅藻遗骸的目的是使Al2O3、Fe2O3溶解,从硅藻遗骸中浸取出Al3+和Fel3+
②步骤II中涉及铝元素的离子方程式为Al3++4OH-=AlO2-+2H2O(或Al3++3OH-=Al(OH)3↓? Al(OH)3+OH-=AlO2-+2H2O),Al3+与OH-的反应与量有关。
③步骤III中不能用HCl代替CO2;HCl不好控制用量,HCl过量Al(OH)3↓会溶解,HCl少量,AlO2-不能完全沉淀。该步骤所得滤液中存在的离子有:阳离子:Na+、 H+?阴离子:CO32-、HCO3-、OH-、SO42-。根据电荷守恒即有:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+2c(SO42-)。向该滤液中滴加少量NaOH溶液,消耗H2CO3、CO32-增大,所以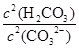 =
=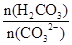 比值变小
比值变小
(3)Al(OH)3可用作阻热材料,利用Al(OH)3受热分解,使温度降低。3的分离与制备,物质分离,方程式书写等结合在一起考查
本题难度:一般
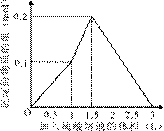
5、选择题 在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1 mol/L的H2SO4溶液,下列图象中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是(?)
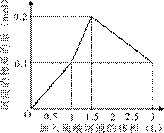 ?
?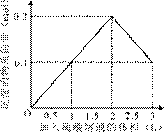 ?
?
A ?B
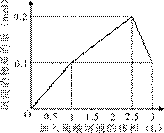 ?
?
C? D
参考答案:A
本题解析:略
本题难度:一般