1、选择题 世界上60%的镁是从海水中提取的,其主要步骤如下:①把贝壳制成石灰乳 ②在海水中加入石灰乳,过滤,洗涤沉淀物 ③将沉淀物与盐酸反应,结晶、过滤 ④在氯化氢热气流中干燥晶体 ⑤电解上述晶体的熔融物。下列说法不正确的是? ( )。
A.镁元素在元素周期表中位于第3周期,ⅡA 族
B.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净
C.在氯化氢热气流中干燥晶体的目的是抑制MgCl2水解
D.步骤⑤也可以采用电解该晶体水溶液的方法
参考答案:D
本题解析:D项中操作的反应化学方程式是MgCl2+2H2O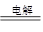 ?Mg(OH)2↓+
?Mg(OH)2↓+
H2↑+Cl2↑,即电解MgCl2溶液得不到镁。
本题难度:一般
2、选择题 常温下,能与SiO2发生反应的物质是(?)
A.烧碱
B.氢氟酸
C.水
D.氧化钙
参考答案:AB
本题解析:常温下能与二氧化硅反应的只有烧碱与氢氟酸,氧化钙可在高温下与二氧化硅反应,水在高温下也不与二氧化硅反应。
本题难度:简单
3、选择题 当我们把若干块普通玻璃叠加,或从侧面看这块玻璃时,它都是淡绿色的。因为普通玻璃中含有二价铁。工厂中也可以在玻璃中加入氧化钴而制得蓝玻璃,加入氧化亚铜而制得红玻璃。下列有关玻璃的说法错误的是
[? ]
A.普通玻璃的组成可表示为Na2O・CaO・6SiO2
B.氢氟酸能腐蚀玻璃是因为它是最强的无氧酸
C.钢化玻璃的机械强度比普通玻璃大4~6倍
D.石英玻璃的膨胀系数相当于普通玻璃的1/18
参考答案:B
本题解析:
本题难度:简单
4、选择题 海水的综合利用可以制备金属钠和镁,其流程如下图所示:
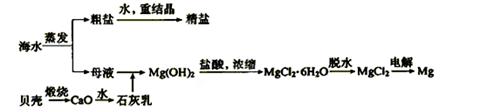
下列说法不正确的是(?)
A.要检验母液中是否含氯离子应当用硝酸酸化的硝酸银溶液进行实验
B.上述流程中所有反应都是非氧化还原反应
C.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2= Mg(OH)2+Ca2+
D.不用电解MgO来制取镁是因为MgO熔点高,能耗大
参考答案:B
本题解析:母液中加入石灰乳生成氢氧化镁,离子方程式为Mg2++Ca(OH)2= Mg(OH)2+Ca2+,C正确;检验母液中Cl-用硝酸银溶液和稀硝酸,A正确;上述流程中氯化镁电解生成镁和氯气是氧化还原反应,B错误;工业上电解氯化镁制镁而不是电解氧化镁制镁,因氧化镁熔点高,D正确。
点评:石灰乳是氢氧化钙的悬浊液,书写离子方程式时不能拆开;石灰水是氢氧化钙水溶液,书写离子方程式时,需拆开。
本题难度:一般
5、填空题 铬酸铅俗称铬黄,不溶于水。广泛用于涂料、油墨、漆布、塑料和文教用品等工业。实验室模拟工业上用铬污泥(含有Cr2O3、Fe2O3、A12O3、SiO2等)制备铬黄的工艺流程如下:
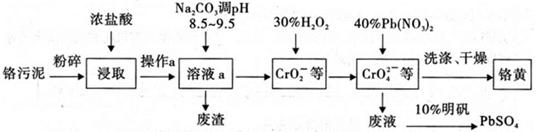
(1)将铬污泥粉碎的目的是?,操作a的名称为?;
(2)废渣的主要成分是A1(OH)3和Fe(OH)3。已知25℃时,A1(OH)3的Ksp=1.3×10-33,则该温度下反应Al3++3H2O Al(OH)3+3H+的平衡常数为?(保留两位有效数字);
Al(OH)3+3H+的平衡常数为?(保留两位有效数字);
(3)写出加入30%H2O2过程中发生的离子反应方程式:?;
(4)实验室洗涤铬黄沉淀的方法:?;
(5)写出浓盐酸与A12O3反应的离子方程式:?。
参考答案:(14分)(1)增大接触面积,提高浸取率(2分)?过滤(2分)
(2)7.7×10-10(2分)
(3)2CrO2-+3H2O2+2OH-=2CrO42-+4H2O(3分)
(4)加蒸馏水浸没铬黄沉淀,等蒸馏水流尽后,再重复操作1~2次(3分)
(5)Al2O3+6H+=2Al3++3H2O(2分)
本题解析:(1)铬污泥含有固体反应物,固体粉碎的目的是增大固体反应物的表面积,增大化学反应速率,提高铬等元素的浸取率;氧化铬、氧化铁是碱性氧化物,易溶于过量的浓盐酸,得到含有CrCl3、FeCl3的溶液,氧化铝是两性氧化物,溶于过量的浓盐酸,得到含有AlCl3的溶液,二氧化硅是酸性氧化物,不溶于盐酸,则操作a为过滤,目的是除去SiO2;(2)溶液a中加入适量Na2CO3调pH8.5~9.5时,碳酸根离子与氢离子容易反应生成二氧化碳和水,碳酸根离子与铁离子容易发生双水解反应,生成氢氧化铁沉淀和二氧化碳,碳酸根离子与铝离子容易发生双水解反应,生成氢氧化铝沉淀和二氧化碳,再次过滤所得废渣的主要成分是A1(OH)3和Fe(OH)3,碳酸根离子水解促进铬离子水解,但是铬离子的水解没有进行到底,导致滤液中主要成分是NaCrO2、NaCl等的溶液;由于25℃时H2O H++OH-,则Kw=1.0×10-14;由于Al(OH)3(s)
H++OH-,则Kw=1.0×10-14;由于Al(OH)3(s)  Al3++3OH-,则Ksp[Al(OH)3]=c(Al3+)?c3(OH-)=1.3×10-33;由于Al3++3H2O
Al3++3OH-,则Ksp[Al(OH)3]=c(Al3+)?c3(OH-)=1.3×10-33;由于Al3++3H2O Al(OH)3+3H+,则K=
Al(OH)3+3H+,则K=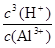 =
=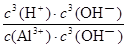 =
=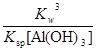 =
=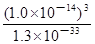 ≈7.7×10-10;
≈7.7×10-10;
(3)pH=8.5~9.5时,溶液呈碱性,CrO2-变为CrO42-是氧化反应,铬元素的化合价由+3价升为+6价,由此推断H2O2是该反应的氧化剂,氧元素由―1价降为―2价,则还原产物是水,根据电子、电荷、原子个数守恒原理配平,该过程的离子方程式为2CrO2-+3H2O2+2OH-=2CrO42-+4H2O;(4)洗涤沉淀时,一般是向沉淀中加蒸馏水至浸没铬黄沉淀,等蒸馏水流尽后,再重复操作1~2次;(5)氧化铝是两性氧化物,盐酸是强酸溶液,二者反应生成氯化铝和水,氯化铝是易溶易电离的盐,则该反应为Al2O3+6H+=2Al3++3H2O。
本题难度:困难